Концентрация - ион - кальций
Cтраница 3
При совместном присутствии Са3 ( РО4) 2 и НгУ2 концентрация ионов кальция определяется как величиной условного произведения растворимости, так и величиной условной константы нестойкости. [31]
По полученным данным опыта строят выходную кривую, отражающую изменение концентрации ионов кальция в отдельных порциях фильтрата. По этой кривой определяют объем промывного раствора ( Vmax), соответствующий максимальной концентрации элемента в зоне. Расчет константы обмена проводят по формуле, приведенной на стр. [32]
По полученным данным опыта строят выходную кривую, отражающую изменение концентрации ионов кальция в отдельных порциях фильтрата. По этой кривой определяют объем промывного раствора ( Ушах), соответствующий максимальной концентрации элемента в зоне. Расчет константы обмена проводят по формуле, приведенной на стр. [33]
Вычисление по табл. 14 дает правильные результаты при условии, если концентрации ионов кальция и бикарбоната приблизительно равноэквивалентны. Вычисление становится ненадежным, если вода содержит значительное количество бикарбонатов натрия и магния, а также хлоридов и сульфатов. В мягких водах с карбонатной жесткостью менее 6 вычисление по табл. 14 также не дает точных результатов. [34]
В 0 10 М растворе СаС12 концентрация ионов кальция равна сумме концентраций ионов кальция из хлорида и фторида кальция. [35]
Во многих артезианских водах содержание бикарбонатов превышает количество, эквивалентное сумме концентраций ионов кальция и магния. Поэтому можно считать, что такая вода содержит также бикарбонат натрия и обладает только карбонатной жесткостью. Содержание сульфатов часто бывает незначительным. [36]
Комплект, в котором используется метод версенейт, позволяет быстро определить концентрацию ионов кальция и магния. Титрованный раствор содержит химические соединения, вступающие в реакцию с кальцием и магнием и образующие в - результате этого комплексные ионы. Конец титрования определяют при помощи индикатора, изменяющего цвет от красного до голубого, когда удаляются последние ионы кальция и магния. Для обеспечения соответствующего уровня рН перед титрованием добавляется буферный раствор. [37]
Для перерасчета - жесткости на кальций можно применять коэффициент, вычисленный из соотношения концентраций ионов кальция и магния в воде. Это соотношение более или менее постоянно в каждом конкретном случае и не меняется при подготовке воды подкислением. [38]
При этом повышается концентрация карбонатов в воде, что приводит к пропорциональному уменьшению концентрации ионов кальция. [39]
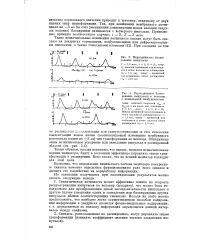 |
Периодическое блокирование импульсов в волокне с пониженной возбудимостью. [40] |
Так, при понижении мембранного потенциала на - 5 мв ( за счет уменьшения концентрации ионов кальция снаружи волокна) блокировки начинаются с четвертого импульса. Приведенные примеры соответствуют случаю: i 3, Т 3 мсек. [41]
Таким образом, для определения остаточной жесткости фильтрата при Na-катионировании воды данного состава достаточно знать концентрации ионов кальция, магния и натрия в регене-рационном растворе. [42]
Если процесс абсорбции протекает в условиях избытка углекислоты, то его движущую силу целесообразно выразить через концентрации иона кальция в растворе. [43]
В этом случае влияние солей кальция на растворимость осадка резко отличается от влияния фторидов При увеличении концентрации ионов кальция в 10 раз концентрация ионов фтора уменьшается всего в 1 103 1 раза. При увеличении же в 10 раз концентрации ионов фтора концентрация ионов кальция уменьшится в 102100 раз. [44]
Данные таблицы говорят о том, что даже в концентрированных растворах фосфорной кислоты может в основном кристаллизоваться гипс, если концентрация ионов кальция значительно превосходит концентрацию 804-ионов. Если же CaO / SO3 меньше единицы, образуется полугидрат. Роль отношения СаО SO3, как видим, достаточно существенна и в известной мере перекрывает действие концентрации Н3РО4 и температуры. [45]
Страницы: 1 2 3 4