Концентрация - свободный ион
Cтраница 1
Концентрации свободных ионов РиО и Fe2 приблизительно равны стехиометрическим концентрациям, поскольку константы гидролиза этих ионов малы по сравнению с концентрацией Н - ИОНОБ. [1]
Концентрация свободных ионов радиоактивного изотопа в свою очередь связана с его состоянием в растворе. Так, например, если радиоактивный изотоп участвует в реакциях комплексообра-зования или гидролизуется и образует нерастворимые соединения, то концентрация его свободных ионов уменьшается, потенциал выделения смещается в отрицательную сторону и соответственно уменьшается выделение радиоактивного изотопа на металле. В некоторых случаях оказывается возможным при помощи электрохимического метода отличить истинноколлоидное состояние от псевдоколлоидного. [2]
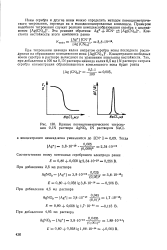 |
Кривые потенциометрического титрования О IN раствора AgNO3 IN раствором NaCl. [3] |
Концентрацию свободных ионов серебра в растворе вычисляют по уравнению константы нестойкости. [4]
Концентрацию свободных ионов железа можно представить ( как это было сделано на стр. [5]
Концентрацию свободных ионов водорода h легко определить потенциометрически, используя водородный, хингидрон-ный или стеклянный электроды ( см. гл. [6]
Концентрацию свободных ионов железа можно представить ( как это было сделано на стр. [7]
Известна концентрация свободных ионов металла и, следовательно, также свободных лигандов. [8]
Измеряется концентрация свободных ионов металла. [9]
При этом концентрация свободных ионов определяется не только мономолекулярным равновесием, но и бимолекулярным взаимодействием ионов разных полимерных цепей. [10]
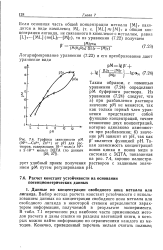 |
Графики зависимости рМ ( М2 - Си2, Zn2 от рН для растворов, содержащих 10 - 3 моль / л М2 а 2 - Ю-3 моль / л ЭДТА ( по данным. [11] |
Данные по концентрации свободного иона металла или лиганда. Выбор метода расчета констант устойчивости с использованием данных по концентрации свободного иона металла или свободного лиганда в некоторой степени определяется характером информации, получаемой в результате эксперимента. В табл. 7.1 перечислен ряд наиболее часто применяемых методов расчета и даны ссылки на разделы настоящей книги, в которых можно найти информацию по ограничениям каждого из методов. [12]
Следовательно, концентрация свободного иона металла М убывает по мере увеличения значения PMY и уменьшения исходной концентрации металла. [13]
Вследствие этого концентрация свободных ионов трехвалентного железа резко уменьшается и окисления дифениламина не происходит. [14]
Примерная оценка концентрации свободных ионов платины в растворах комплексов платины может быть сделана, исходя из приведенных на стр. Эти значения чрезвычайно малы. Если учесть большую прочность комплексов Pt ( IV) по сравнению с производными Pt ( II), то концентрация ионов [ Pt4 ] должна быть еще меньше, и совершенно естественно, что такие концентрации вряд ли могут обеспечить достаточно быстрое установление потенциала. Тем самым ясно, что в случае очень прочных комплексов, характеризующихся очень малыми значениями суммарной константы вторичной диссоциации, установление потенциала должно идти не через простые Ионы, а иными путями, которые будут несколько более подробно рассмотрены ниже. [15]
Страницы: 1 2 3 4