Концентрация - водородный ион
Cтраница 2
Концентрация водородных ионов ( рН) может быть определена электролитическим и колориметрическим способами. [16]
Концентрация водородных ионов обозначается величиной рН, которая является отрицательным логарифмом ( десятичным) концентрации Н в растворе. [17]
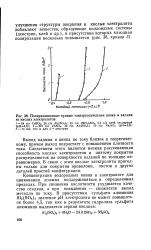 |
Поляризационные кривые электроосаждения цинка и кадмия из кислых электролитов. [18] |
Концентрация водородных ионов в электролите для цинкования должна поддерживаться в определенных пределах. При снижении кислотности ухудшается качество осадков, а при повышении - снижается выход металла по току. [19]
Концентрация водородных ионов играет большую роль при электроосаждении металлов, особенно выделяющихся при электроотрицательных потенциалах из растворов простых и некоторых комплексных солей. [20]
Концентрация водородных ионов ( рН) играет важную роль во многих явлениях и процессах. Многие химические процессы протекают в желательном направлении при каком-то одном его значении, которое поэтому необходимо поддерживать постоянным. Существуют растворы, сохраняющие более или менее постоянное значение рН, несмотря на добавление кислоты или щелочи; эта способность называется буферностью. Буферную емкость раствора можно определить как число эквивалентов b щелочи ( или кислоты), необходимое для изменения его рН на единицу. [21]
Концентрация водородных ионов существенно влияет на развитие микроорганизмов. [22]
Концентрация водородного иона ( так называемого рН) является свойством эфемерным. [23]
Концентрация водородных ионов в растворе может непосредственно и косвенно влиять на скорость коррозии металлов. В первом случае при коррозии с водородной или кислородной деполяризацией уменьшение рН электролита ( увеличение концентрации Н - ионов) способствует более легкому протеканию катодного процесса, повышению скорости коррозии. Косвенное ( непрямое) влияние рН на коррозию обнаруживается в изменении растворимости продуктов коррозии в данной коррозионной среде, что зачастую приводит к образованию на поверхности корродирующего металла защитных пленок. [24]
Концентрация водородных ионов является существенным фактором и в жизни озера. Течение многих биохимических и других процессов обусловлено определенной концентрацией водородных ионов. [25]
Концентрация водородных ионов вводных растворах кислот и щелочей является показателем свойств растворов. Измерение этого показателя имеет важное значение. [26]
Концентрация водородных ионов, при которой активность какого-либо энзима является наиболее высокой, называется оптимальной концентрацией для данного энзима. [27]
Концентрация водородных ионов ( рН) может быть определена электрометрическим и колориметрическим способами. Колориметрические методы менее точны, но значительно более просты и нашли широкое применение в лабораторной и заводской практике. [28]
Концентрация водородных ионов ( рН) в водных растворах кислот и щелочей является показателем свойств растворов. Измерение этого показателя в целом ряде технологических процессов различных производств имеет важное эксплуатационное значение. [29]
Концентрация водородных ионов в электролите мала и для их перехода из ионного IB молекулярное состояние необходимо преодолеть высокое перенапряжение. [30]
Страницы: 1 2 3 4