Концентрация - борная кислота
Cтраница 3
Однако с введением борной кислоты в электролит значительно повышается микротвердость пленки, что увеличивает ее износостойкость. С ростом концентрации борной кислоты в электролите до 2 г / л наблюдается значительное повышение микротвердости. При дальнейшем повышении концентрации борной кислоты значение микротвердости резко падает. [31]
Воздух с объемным расходом 10 л / мин аспирируют через фильтр, помещенный в фильтродержатель. Для определения концентрации борной кислоты и борного ангидрида на уровне 1 / 2 ПДК следует отобрать 40 л воздуха. [32]
Применяется 0 5 % раствор резацетофенона в концентрированной серной кислоте. Прямая пропорциональность между концентрацией борной кислоты и интенсивностью люминесценции наблюдается в интервале концентрации кислоты от 0 0004 до 320 мкг / мл. С увеличением количества воды в анализируемом растворе интенсивность люминесценции уменьшается. [33]
Антраценовый синий СВГ [31] в среде 85 % раствора H2SO4 с ионами борной кислоты образуют комплекс, люминесцирующий красным светом. Интенсивность люминесценции прямо пропорциональна концентрации борной кислоты в растворе в интервале 0 001 - 0 02 мкг / мл бора. Определению мешают ионы Fe3, VO f, MoOf -, Ti4, а также F -, CrOl -, МпОГ и NO - Г - Метод применим для анализа сплавов на основе магния, алюминия и цинка. Навеску стружки сплава 0 1 г помещают в кварцевую колбу, содержащую 10 мл воды. Колбу присоединяют к обратному холодильнику для избежания потерь бора и осторожно приливают серную кислоту и под конец 30 % раствор H2O2 до полного растворения карбидов. Отбирают 5 мл, добавляют 0 15 мл 0 1 % - ного раствора реагента в концентрированной серной кислоте и через 20 мин измеряют интенсивность люминесценции комплекса. [34]
Например, при 18 в 0 25 ( 0 5; 0 75) М растворе константа диссоциации становится равной 26 ( 119; 408) 10 - 10 соответственно. В разбавленных растворах ( концентрация борной кислоты ниже 0 1 М) константа диссоциации не зависит от концентрации. [35]
Ионы церия ( III) и лантана ( III) также реагируют с БПКК, однако они образуют комплексы меньшей прочности. Влияние лантана устраняется повышением концентрации борной кислоты до 0 05 М, а влияние церия - введением перекиси водорода, окисляющей Се111 до Ceiv. В этих условиях около 77 % иттрия связывается в комплекс с БПКК. [36]
РА и 5.88 % MgO концентрация борной кислоты равна 0.92 % вместо 19.81 % при отсутствии мономагнийфосфата. [37]
 |
Изменение концентраций борной кислоты и ионов калия в процессе работы реакторов ВВЭР-1000. [38] |
После распада СССР эти нормы продолжают действовать во всех странах, где эксплуатируются реакторы ВВЭР. На рис. 14.1.2 представлена область изменения концентраций борной кислоты и ионов калия в процессе работы на мощности реакторов ВВЭР-1000. Как видно из графика только до выхода на постоянное значение верхней границы концентрации ионов калия в теплоносителе возможно поддержание постоянного требуемого высокотемпературного значения рН, что при существующих технологиях поддержания водно-химического режима является оптимальным. При повышении концентрации изотопа бора-10 в борной кислоте в 3 раза появляется возможность работы реакторов с водой под давлением в области постоянного значения высокотемпературного рН, так же значительно уменьшились бы все системы переработки теплоносителя, деба-лансных вод и других водных потоков. Повысилась бы надежность систем безопасности, так как отпадает необходимость поддержания концентрации борной кислоты близкой к пределу ее растворимости. [39]
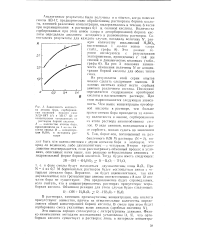 |
Зависимость количества атомов бора, сорбированных единицей емкости смол ЭДЭ-10П ( / и АВ-17 ( 2 от концентрации насыщающих их. [40] |
На рис. 3 показана зависимость изменения величины N от концентрации борной кислоты для обоих типов смол. [41]
Наиболее широко в производстве сухих электролитических конденсаторов для формовки при всех напряжениях применяются растворы борной кислоты с добавками буры, боратов аммония или аммиака. В этих электролитах изменение напряжения искрения и электропроводности при изменении напряжения формовки достигается варьированием концентрации борной кислоты и щелочных добавок. [42]
Точно такую же ионную проводимость аниона имеют гексабораты кобальта и марганца, растворенные в 3 % - ной борной кислоте, что указывает на присоединение борной кислоты к тетра-боратам переходных металлов. При этом образуется, по-видимому, гексаборат-ион, но полнота превращения в каждом отдельном случае различна и зависит от концентрации борной кислоты и природы аниона. [43]
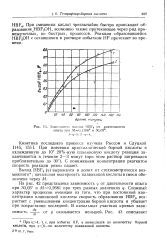 |
Зависимость выхода HBF4 от длительности опыта при УИ 0 1388 и 30 05. [44] |
На рис. 42 представлена зависимость с. Сложный характер процессов очевиден из того, что при постоянной концентрации плавиковой кислоты скорость образования HBF4 возрастает с уменьшением концентрации борной кислоты и убывает при возрастании последней. [45]
Страницы: 1 2 3 4