Концентрация - реагирующий компонент
Cтраница 1
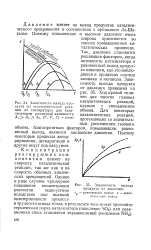 |
Зависимость выхода продукта ( х экзотермической реакции от температуры для катализаторов различной активности Ai AZ А3, ( Т, Р, Q const. [1] |
Концентрация реагирующих компонентов влияет на скорость каталитической реакции, так же как и на скорость обычных химических превращений. [2]
Концентрация реагирующих компонентов влияет на скорость каталитической реакции так же, как и на скорость обычных химических превращений. Однако чрезмерное повышение концентрации реагентов недопустимо вследствие ряда причин. [3]
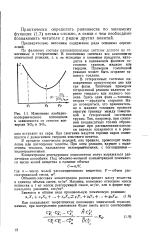 |
Изменение изобарно-изотермического потенциала в зависимости от степени конверсии SO2 в SO3. [4] |
Концентрации реагирующих компонентов могут выражаться различными способами. [5]
Концентрация реагирующих компонентов в сырье должна быть максимальной, а концентрация насыщенных парафиновых углеводородов нормального строения - минимальной. [6]
Изменение концентраций реагирующих компонентов, а также изменение потенциала в процессе окислительно-восстановительного титрования изучено экспериментально и в ряде случаев может быть рассчитано на основе формулы Нернста. [7]
Изменения концентраций реагирующих компонентов, вызываемые присутствием посторонних, но взаимодействующих с ними веществ ( в данном случае маскирующих агентов), учитываются при пользовании реальными константами равновесия. Поэтому реальные константы удобны для выяснения возможностей маскирования. Если реальная константа Кс - г в условиях, в которых осуществляют маскирование, настолько меньше константы Кг; что неравенства (17.2), (17.4), (17.6), (17.8) изменяются на противоположные, осуществляется маскирование мешающего вещества. [8]
Распределения концентраций реагирующих компонентов вблизи плоской поверхности реакции могут быть выражены через общее количество вещества, реагирующего на единице поверхности пламени в единицу времени. [9]
Чем ниже концентрация реагирующих компонентов, тем болы образуется этилентлнколя и тем ниже ныход окиси этилена. Бол благоприятные условия создаются, если в колонну ( насалочш или тарельчатую), к которой проводится обрабочка этшюихлоргл рина щелочью, снизу нводить нар п подогревать 4 - 6 % - ный рЕ твор этиленхлоргидрина до температуры кипении азготропн СМРСИ - чтиленхлоргидрипа л поды. При этом содержание этшк хлоргндрина в нарах повышается до 41 % и во взаимодействие щелочью, орошающей колонну, истуиает не разбавленный, а кс центрированный этиленхлоргндрин. Таким г разом, реакция протекает фактически между концентрированны. [10]
В зависимости от концентраций реагирующих компонентов это соединение существует либо в растворимой форме, либо выпадает в осадок. В последующие годы состав ферроцианида молибдена был исследован спектрофотометрическим [5-7], потенциометрическим [.], кондуктометрическим [8,9], амперометри-чесним [ 9 - И ] методами, а также методами объемного [12] и весового [13] анализа. В целях количественного анализа реакция образования ферроцианида молибдена была использована рядом авторов [14,15] для фотометрического определения последнего. [11]
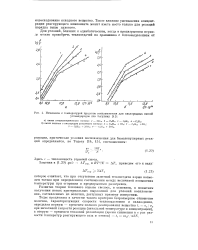 |
Изменение е температурой пределов воспламенения для кислородных смесей. [12] |
Такое влияние уменьшения концентрации реагирующего компонента может иметь место только для реакций порядка выше нулевого. [13]
Это дает возможность выразить концентрации реагирующего компонента через относительное изменение температуры. [14]
Это дает возможность выразить концентрации реагирующего компонента через относительное изменение температуры. Согласно (12.22), если реакция развивается вблизи 7 акс, то она должна происходить н смеси, состоящей в основном из продуктов сгорания. [15]
Страницы: 1 2 3 4