Концентрация - сернокислая медь
Cтраница 1
Концентрация сернокислой меди в ванне может быть тем выше, чем выше температура электролита и чем интенсивнее перемешивание раствора. Повышение температуры сернокислого электролита приводит к снижению и без того малой катодной поляризации и к образованию более грубого покрытия. Однако, если процесс осаждения совершается при высокой катодной плотности тока, то повышение температуры необходимо, чтобы повысить скорость диффузии ионов меди из глубины электролита в прикатодный слой. С этой же целью вводится перемешивание раствора. [1]
Концентрацию сернокислой меди выбирают в соответствии с принятыми плотностью тока и концентрацией серной кислоты в ванне. [2]
Нежелательное уменьшение концентрации сернокислой меди, происходящее во всем объеме электролита, еще заметнее обнаруживается в при-катодном слое. [3]
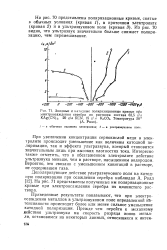 |
Анодные и катодные поляризационные кривые при электроосаждении серебра из раствора состава 62 5 г. л KAg ( CN2 20 г / л KCN, 15 г / л К2СО3. Температура 20 ( А. Ролл. [4] |
При увеличении концентрации сернокислой меди в электролите происходит уменьшение как величины катодной поляризации, так и эффекта ультразвука, который становится значительным лишь при высоких плотностях тока. Интересно также отметить, что в обезгаженном электролите действие ультразвука меньше, чем в растворе, насыщенном водородом. Вероятно, это связано с уменьшением кавитаций в растворе, не содержащем газа. [5]
При длительной работе, особенно при перемешивании воздухом, в электролите повышается концентрация сернокислой меди и снижается содержание серной кислоты. [6]
По мере хода электролиза состав раствора изменяется, в нем накапливается сернокислый цинк, а концентрация сернокислой меди падает. Если необходимо вести процесс длительное время, то концентрация меди в растворе поддерживается искусственно добавлением медного купороса. [7]
Они установили, что увеличение удельной мощности поля ( примерно до 2 - 2 5 вт / см2) существенно снижает катодную поляризацию. Увеличение в электролите концентрации сернокислой меди уменьшает катодную поляризацию и снижает деполяризующее действие ультразвука, проявляющееся лишь при высоких плотностях тока. [8]
 |
Схема гальванического элемента. [9] |
Причем, на сколько грамм-эквивалентов уменьшится в весе цинковая пластинка, на столько грамм-эквивалентов увеличится медная. Концентрация сернокислого цинка у цинкового электрода увеличивается, а концентрация сернокислой меди у медного электрода на столько же уменьшается. [10]
Медь из кислых растворов может быть выделена также и электролизом. Для экономичного проведения этого процесса желательно, по возможности, повысить концентрацию сернокислой меди в кислой ванне. После регенерации в растворе остается меньше 0 03 % меди. Кислота, отделенная от меди, снова поступает в производство. Регенерация меди путем электролиза имеет преимущества и недостатки по сравнению о выделением меди из кислого раствора в виде гидроокиси меди. [11]
Примером обратимого гальванического элемента является так называемый элемент Даниэля, в котором используются медный электрод, погруженный в раствор сернокислой меди ( Си5О4), и цинковый электрод, погруженный в раствор сернокислого цинка ( 2п5О4); растворы разделены пористой перегородкой, проницаемой для ионов. Если осуществить процесс в обратном направлении, пропуская через электролит электрический ток от внешнего источника, то процесс обращается - на цинковом электроде отлагается цинк и концентрация сернокислого цинка в растворе электролита уменьшается, а медный электрод растворяется и концентрация сернокислой меди в растворе электролита увеличивается. [12]
Рассмотрим в первую очередь явление диффузии, имеющее большое значение в процессах жизнедеятельности организмов. Если в цилиндр налить раствор сернокислой меди ( CuSO4), имеющий голубой цвет, и затем на поверхность этого раствора налить осторожно слой дистиллированной воды, то первое время между раствором и водой наблюдается резкая граница. Со временем эта граница постепенно размывается. Благодаря тепловому движению, молекулы сернокислой меди будут проникать в слой воды, в то время как молекулы воды в силу того же движения проникают в раствор сернокислой меди. Это взаимное проникновение с течением времени приводит к тому, что, наконец, концентрация сернокислой меди будет всюду одинакова. [13]
На рис. 2 представлены кривые распределения серно-кислой меди в процессе электролиза во всем межэлектродном пространстве от анода до катода. Режимы электролиза указаны на рисунках. Из рис. 2 видно, что анодный и катодный процессы не являются зеркальными изображениями друг друга. В прианодном пространстве нарастание концентрации идет интенсивнее, чем убывание концентрации у катода. Концентрация электролита у электродов при неизменной плотности тока постепенно изменяется. Градиент концентрации также изменяется во времени как у электрода, так и в объеме раствора. Все это является характерными чертами нестационарного электролиза. Из него видно, что рост концентрации сернокислой меди зависит от режима электролиза. Можно подобрать такие условия, что на аноде выпадают кристаллы серно-кислой меди. [14]
Страницы: 1