Концентрация - неионизированная молекула
Cтраница 1
 |
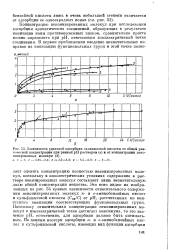
Зависимость относительного содержания неионизированных молекул Срщ / С от рН растворов. [1] |
Концентрация неионизированных молекул Сни может быть рассчитана по константе ионизации функциональных групп вещества Ки для экспериментально определенной величины рН раствора. [2]
Концентрацию неионизированных молекул при исследовании адсорбции ароматических соединений, образующих в результате ионизации ионы противоположных знаков, сравнительно просто можно определить при рН, отвечающем изоэлектрической точке соединения. [4]
В первом случае концентрация неионизированных молекул в растворе определяется только наибольшей константой ионизации. [5]
Зная, что концентрация неионизированных молекул воды ( равная 55 50 - 1 10 - 7) в 555 млн. раз превосходит концентрацию ионизированных молекул, ее считают величиной постоянной. [6]
Затрата Н на этот процесс, очевидно, равна концентрации неионизированных молекул Н3Р - О4 в растворе. [7]
При изменении концентрации ионов Н или ионов ОН степень ионизации воды будет соответственно изменяться, но концентрация неионизированных молекул будет при этом оставаться практически постоянной. [8]
Следовательно, константа ионизации есть отношение произведения концентраций ионов, на которые распадается электролит, к концентрации неионизированных молекул электролита. Величина ее характеризует способность электролита диссоциировать на ионы. Чем больше величина константы ионизации, тем больше электролит распадается на ионы. [9]
В разбавленных растворах вода находится в огромном избытке, а так как ионизация ее ничтожно мала, концентрацию неионизированных молекул воды можно считать практически постоянной, не изменяющейся при любом смещении равновесия гидролиза. [10]
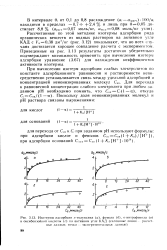 |
Изотермы адсорбции.. - толуидина ( о, фенола ( б, н-нитрофенола ( в и оксибен. чойиой кислоты ( с на активном угле КАД ( сплошные линии расчетные данные, точки - экспериментальные данные. [11] |
При вычислении изотерм адсорбции слабых электролитов по константе адсорбционного равновесия и растворимости непосредственно устанавливается связь между удельной адсорбцией и концентрацией неионизированных молекул Снн. [12]
 |
Схема самоионизации воды. [13] |
В 1 л воды содержится ( 1000: 18 016) 55 50 моль воды, из которых I-IO 7 моль находится в ионизированном состоянии, а остальное количество воды - в виде неионизированных молекул. Зная, что концентрация неионизированных молекул воды ( равная 55 50 - 1 10 - 7) в 555 млн. раз превосходит концентрацию ионизированных молекул, ее считают величиной постоянной. [14]
Такой процесс называется гидролизом по аниону, так как анион вступает в реакцию обменного разложения воды и обусловливает накопление в растворе гидроксид-ионов. Он продолжается до тех пор, пока в системе не установится равновесие между концентрацией неионизированных молекул уксусной кислоты и ее ионами. А так как уксусная кислота слабая ( / Сдио1 74 - 10 - 5), то концентрация ионов ЮН - ] в растворе будет значительной. [15]
Страницы: 1 2