Концентрация - нитрат
Cтраница 2
С - концентрация нитратов, определенная по калибровочной кривой, мг / л; V - объем пробы, взятой для анализа, мл. [16]
С - концентрация нитратов, найденная по калибровочному графику, мг / л; У1 - объем первоначальной пробы, взятой для разбавления, мл; К2 - объем пробы после разбавления, мл. [17]
При повышении концентрации нитратов и температуры уменьшается время до начала появления растрескивания при данном напряжении. [18]
При увеличении концентрации нитратов ( NOJ и Mes) понижается степень диссоциации и гидратации редкоземельных металлов, сдвигая равновесие в сторону образования экстрагируемых форм. Этот процесс при определенных концентрациях солей начинает доминировать, в результате чего подавляется инверсия и начинает возрастать степень разделения, причем, чем выше степень дегидратации, тем больше степень разделения. [19]
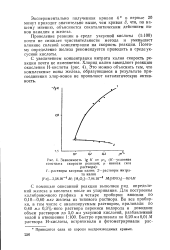 |
Зависимость lg К от константа скорости реакции. ( J. ионная сила. [20] |
С увеличением концентрации нитрата калия скорость реакции почти не изменяется. Это можно объяснить тем, что комплексные ионы железа, образующиеся в результате присоединения хлор-ионов не проявляют каталитическую активность. [21]
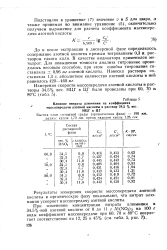 |
Влияние нитрата алюминия на коэффициент. [22] |
При изменении концентрации нитрата алюминия в 34 5 % - ной азотной кислоте от 0 до 11 г А1 ( МО3) з на 100 г воды коэффициент массопередачи при 60, 70 и 80 С возрастает соответственно на 12, 25 и 45 % ( см. таил. [23]
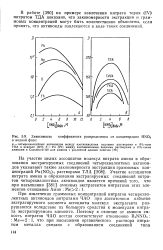 |
Зависимость коэффициента распределения от концентрации HNO3 в водной фазе. [24] |
При извлечении граммовых концентраций нитратов четырехвалентных актиноидов нитратами ЧАО при достаточном избытке экстрагируемого элемента ассоциаты молекул экстрагента разрушаются вследствие их большого сродства к молекулам нитрата экстрагируемого элемента. [25]
Однако при концентрациях нитратов 10 - 4 моль / дм3 соответствующие реакции протекают не полностью, что затрудняет определение. [26]
 |
Поверхность образца после фосфатирования в растворе с добавкой нитрата ртути ( на поверхности видны осажденные капельки ртути. [27] |
При повышении: концентрации нитрата ртути с 0 5 до 50 г / л продолжительность выделения водорода возрастает с 10 мин до 2 ч и более. Структура фосфатной пленки становится неравномерной. [28]
По мере повышения концентрации нитратов в растворе, содержащем первичные фосфаты железа, марганца или цинка ( 30 - 35 г / л), размеры кристаллов фосфатов, составляющих фосфатную пленку, уменьшаются, а обусловленная ими кристаллическая структура изменяется: шероховатость исчезает, пленка становится гладкой, блестящей, более тонкой и приобретает темно-синюю окраску. На поверхности сначала образуются небольшие участки фосфато-окисной пленки, которая при дальнейшем повышении концентрации нитратов уже полностью покрывает металл. [29]
При значительном увеличении концентрации нитрата ( например, в растворе 1 М NaN03) питтингообразование подавляется. Это объясняется тем, что ионы N01 не попадают в отверстия и не адсорбируются на поверхности питтингов. [30]
Страницы: 1 2 3 4 5