Концентрация - свободный бром
Cтраница 1
Концентрация свободного брома определялась изопиестически ( см. гл. [1]
Система генерации поддерживает концентрацию свободного брома постоянной. Ток, необходимый для генерации, прямо пропорционален количеству использованного брома, а потребление брома зависит от количества SO2, проходящего через ячейку и реагирующего с бромом. [2]
Величина еН сорбента определяется, очевидно, соотношением концентраций свободного брома и бромида. При малой Сщ в сорбенте имеется свободный бром, тогда как с увеличением вонцентрации NtxOH и повышением скорости гидролиза бром отсутствует. В диапазоне изменения концентрации щелочи от 10 до 50 г / л величина еН существенно снижается от 610 до 540 мв. [3]
По условиям производства управлять реакцией синтеза нужно так, чтобы в выходящем из реактора дибромпропане-сырце концентрация свободного брома составляла I г / л и не содержался пропилен. Обеспечить выполнение этого требования стабилизацией соотношения расходов раствора брома в ДБП и пропилена на входе в реактор невозможно из-за непостоянства концентрации брома в исходном растворе. [4]
Потенциал измерительного электрода из благородного металла, равный окислительно-восстановительному потенциалу системы бром-бромид, является мерой концентрации свободного брома в растворе и служит для поддержания этой концентрации на заданном уровне. [5]
Скорость-определяющей стадией обмена в бромоплати-ните оказался процесс аквотации комплекса, так как скорость не зависит от концентрации свободного брома. [6]
Изменение концентрации фона Ре3 на Ъ % приводит к изменению показаний прибора на 2 1 %, При изменении концентрации свободного брома в растворе в пределах 0 - 2 г / л дополнительная погрешность определения бромида составляет 1 1 %, Колебания кислотности раствора в пределах рН - I I приводит к отклонению показаний до 2 % от шкалы прибора. [7]
После окисления всего арсенита в растворе появляется свободный бром и через индикаторные электроды начинает идти ток, обусловленный окислительно-восстановительной системой Вг2 / Вг -; отклонение стрелки гальванометра пропорционально концентрации свободного брома. [8]
Итак, данные кинетических измерений можно интерпретировать, допуская, что скрытый в ионе Вг3 - бром неактивен, остаточная же реакционная способность после израсходования 2 / з общего количества брома обусловлена низкой концентрацией свободного брома, находящегося в равновесии с комплексным ионом. [9]
Реакция бромирования является реакцией второго порядка. Изменение концентрации свободного брома в реакционной системе контролируют с помощью колориметрического метода. [10]
Реакция бромирования является реакцией второго порядка. Изменение концентрации свободного брома в реакционной системе контролируют с помощью колориметрического метода. [11]
При достижении этого условного нуля электролиз автоматически прекращается, и в электролит вносится навеска анализируемого вещества, содержащего углеводород. Происходит количественное бромирование углеводорода, и концентрация свободного брома уменьшается. После окончания бромирования включаются ток и секундомер. Когда индикаторный ток, постепенно увеличиваясь, снова достигнет эталонного значения, соответствующего условному нулю, ток генерации и секундомер выключаются, а продолжительность электролиза ( в секундах) фиксируется. [12]
 |
Изменение тока в цепи ин - ПОСТОЯННЫЙ ПОТбНЦИаЛ ( 0 2 - 0 3 в. [13] |
На графике ( рис. 104) показано изменение величины тока в цепи электродов в ходе титрования. Величина тока нарастает прямо пропорционально увеличению концентрации свободного брома в растворе. [14]
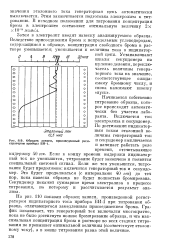 |
Образец записи, произведенный регистратором прибора БИ-1. [15] |
Страницы: 1 2