Концентрация - продукт
Cтраница 3
Изменение концентрации продуктов анодной реакции в растворе может косвенно оказывать влияние на пассивирование электрода. Поскольку растворимость солей ограниченна, чрезмерное накопление ионов металла в приэлек-тродном слое приводит к выделению солей на электроде, экранированию части поверхности и резкому усилению тока на свободной части поверхности, что облегчает пассивирование. Пассивность такого вида называется солевой. Если допустить, что на электроде в пассивном состоянии продолжают параллельно протекать две электрохимические реакции - анодное растворение металла через оксидную пленку и электрохимическое окисление электрода кислородом, то независимость или слабую зависимость скорости анодного процесса от потенциала можно объяснить следующим образом. [31]
Определить концентрацию продукта через 10 мин после подачи сигнала. [32]
Определить концентрацию продукта на выходе через 120 с после окончания импульса при условии, что концентрация вещества R в начальный момент времени равна нулю. Плотность реакционной смеси постоянна. [33]
Меняя концентрацию продуктов гидролиза, можно сместить это равновесие в любом направлении, Так, например, добавле - ние свободной кислоты или свободного основания увеличивает концентрацию негидролизованной соли и таким образом подавляет гидролиз; это используется в одном из методов изучения гидролитического равновесия, стр. [34]
Изменяя концентрацию продуктов гидролиза, можно сместить равновесие его в любом направлении. Если же из раствора гидролизованной соли удалять получающуюся кислоту или основание, то степень гидролиза увеличивается. [35]
Изменяя концентрацию продуктов гидролиза, можно сместить равновесие его в любом направлении. [36]
ХР - концентрация продукта на выходе реактора; SA - стоимость исходного сырья; SY - стоимость единицы объема реактора, исчисляемая с учетом его амортизации. [37]
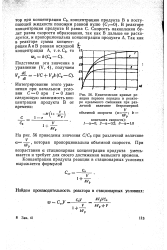 |
Кинетические кривые реакции первого порядка в реакторе идеального смешения при различной величине безразмерной. [38] |
В реакторе концентрация продукта В равна С. Скорость накопления будет равна скорости образования, так как В дальше не расходуется, и пропорциональна концентрации продукта А. [39]
Если бы концентрация продукта на выходе из системы смешения у была единственным регулируемым параметром, то для регулирования системы было бы достаточно изменять проходное сечение только одного из регулирующих клапанов. По условию же требуется обеспечить регулирование расхода растворенного продукта А на выходе из системы. Для регулирования этих двух параметров необходимо воздействовать на расходы концентрата и растворителя одновременно. [40]
Рвх - концентрация продукта на входе ( она равна нулю, если это первый аппарат в каскаде или одиночный аппарат), Р - концентрация продуктов на выходе. [41]
Чтобы уменьшить концентрации продуктов, применяют или удаление их в гетерофазу ( например, растворенную двуокись серы удаляют, продувая раствор азотом), или связывают их в нерастворимые, легколетучие или малодиссоциирующие вещества. Такое связывание означает, что в системе протекает еще по крайней мере одна реакция. [42]
X - концентрация образующего продукта, моль / л, в зависимости от степени превращения реагентов, взятых в соотношении 1: 1 мольн. Кр ( 09) - 30 10 л / моль-с и Кр ( 099) - 150 50 л / моль-с. Индексы 0 9 и 0 99 соответствуют превращению реагентов на 90 и 99 % моль. Как видно, химический процесс синтеза ХБК по реакции хлорирования БК в растворе молекулярным хлором в смеси с азотом протекает достаточно быстро. [43]
С-1 - концентрация продуктов распада, ( 32 - величина постоянная. [44]
Так как концентрация продуктов промежуточных реакций всегда очень мала. [45]
Страницы: 1 2 3 4