Концентрация - пересыщенный раствор
Cтраница 1
Концентрация пересыщенного раствора падает до тех пор, пока не становится равной растворимости вещества при данных условиях. [1]
Отношение концентрации пересыщенного раствора к концентрации насыщения называют коэффициентом пересыщения. [2]
При росте микрокристаллов, как это имеет место в микрокристаллоскопии, концентрация пересыщенного раствора С практически остается постоянной, иными словами, при кристаллизации малого количества вещества значение пересыщения практически остается постоянным, скорость роста кристалла определяется исключительно скоростью притока вещества в граничный слой, а не скоростью отложения частиц на гранях кристалла. [3]
Величина пересыщения может быть вычислена по формуле С - Сн р, где Сп - концентрация пересыщенного раствора, Сн - концентрация насыщенного раствора, р - величина пересыщения. [4]
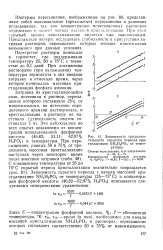 |
Зависимость продолжительности скрытого периода кристаллизации NH4H2PO4 от температуры. Степень пересыщения, % от предельного. [5] |
Изотермы пересыщения, изображенные на рис. 80, представляют собой максимальные ( предельные) пересыщения в условиях исследования, так как концентрацию пересыщенных растворов определял в момент начала массовой кристаллизации. При этом скрытый период кристаллизации является уже завершенным. Представляло интерес исследовать стабильность в присутствии затравки растворов, пересыщение которых меньше максимально возможного при данных условиях. [6]
К - коэффициент, зависящий от коэффициента диффузии D молекул, достигших насыщения, и средней длины диффузионного пути б, т.е. / ( /) / 6; S - поверхность выделившейся твердой фазы; х - концентрация пересыщенного раствора; х - растворимость зародышей кристаллов при данной степени их дисперсности. [7]
Концентрация пересыщенного раствора падает до тех пор, пока не становится равной растворимости вещества при данных условиях. [8]
Если осадок не выделяется, то раствор называют пересыщенным и в нем заторможен процесс кристаллизации. Величину пересыщения вычисляют по формуле Ст - Спр, где Ст - концентрация пересыщенного раствора, Сп - концентрация насыщенного раствора, р - пересыщение. [9]
При охлаждении насыщенного раствора ( рассматривается диаграмма С - Т) тоже говорят о пересыщенной фазе; фазу, возникающую при охлаждении расплава, называют переохлажденной. Пересыщение раствора определяется разностью АСС-Спас, где Снас - концентрация насыщения, С - концентрация пересыщенного раствора. Переохлаждение расплава определяется разностью АГГ-Гпл, где Гпл - температура плавления, Т - температура переохлаждения расплава. [10]
Изложенное может быть распространено и на кристаллизацию из пересыщенных растворов. В этом случае кривая ABC ( см. рис. 118) будет отвечать концентрации насыщенного раствора по отношению к алмазу определенного размера, а кривые р - р - концентрациям пересыщенного раствора. [11]
Изложенное может быть распространено и на кристаллизацию из пересыщенных растворов. В этом случае кривая ABC ( см. рис. 118) будет отвечать концентрации насыщенного раствора по отношению к алмазу определенного размера, а кривые р - р - концентрациям пересыщенного раствора. [12]
Эти требования наиболее полно удовлетворяются при проведении гомогенного осаждения. К осаждаемому раствору добавляют соединения, образующие осадитель только в необходимом для проведения реакции количестве. Для осаждения малорастворимого сульфата применяют, например, диметилсульфат или амидосульфат, для осаждения сульфидов - тиоацетамид или тиокарбамид. На этом же принципе основано применение уротропина для осаждения гидроксидов трехвалентных металлов или тиосульфата, нитрита или смеси иодида и иодата для осаждения легко фильтруемого гидроксида алюминия. Во всех этих методах концентрация L пересыщенного раствора должна быть минимальной. [13]
В известной мере эти характеристики аналогичны. Но есть между ними и некоторые различия. Если относительное пересыщение может быть большим, то относительное переохлаждение в той интерпретации, как это дано уравнением ( 5), не может превысить единицы. Пересыщение в ряде случаев может быть создано мгновенно. Чтобы переохладить раствор, нужно более длительное время. Величина пересыщения растворов труднорастворимых соединений и веществ, умеренно растворяющихся в воде, зависит главным образом от их природы и содержания примесей. Переохлаждение же, кроме того, в известной степени определяется вязкостью, поскольку последняя может существенно зависеть от температуры. Таким образом, вопрос о том, как оценивать отклонение системы от равновесного состояния, связан с условиями проведения и задачами исследования. Разумеется, зная переохлаждение, можно рассчитать пересыщение, и наоборот. В первом случае за концентрацию пересыщенного раствора принимается исходное содержание вещества в жидкой фазе ( концентрация исходного раствора), а за растворимость - его равновесная концентрация при температуре переохлаждения. Во втором случае, когда по пересыщению находится переохлаждение, за исходную температуру принимается та, которая отвечает растворимости, равной концентрации пересыщенного раствора, а за температуру переохлаждения - фактическая температура, при которой определялось пересыщение. Поясним сказанное на примерах. Если же известно, что при 20 раствор нитрата калия пересыщен и абсолютное пересыщение составляет 14.2 г, можно найти переохлаждение. [14]
Страницы: 1