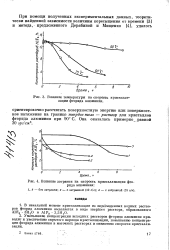
Концентрация - исходный раствор
Cтраница 2
При концентрации исходного раствора х количества образующихся фаз пропорциональны разности ( х - х) для матричной фазы и ( х - х) для низкоконцентрированной фазы. [16]
Пусть концентрация исходного раствора растворимой соли Pb ( NO3) 2 равна с г / мл, а концентрация этого раствора в пересчете на РЬС12 - с / г / мл. Для приготовления эталона было израсходовано V) мл исходного раствора Pb ( NO3h и для приготовления исследуемого образца V2 мл насыщенного раствора РЬСЬ. [17]
Достижение концентрации исходного раствора ( достижение равновесия) наступает быстро после проскока - выходная кривая после проскока резко идет вверх. [18]
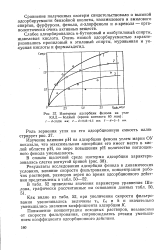 |
Изотермы адсорбции фенола на угле КАД - йодный ( время контакта 60 мин. [19] |
Повышение концентрации исходных растворов, независимо от скорости фильтрования, сопровождались резким уменьшением коэффициента адсорбционного действия. [20]
Повышение концентрации исходного раствора кислоты от 15 до 25 % увеличивает глубину проникновения кислотной пены с активной кислотой в 1 5 - 2 раза. [21]
Уменьшение концентрации исходных растворов фторида алюминия приводит к увеличению скрытого периода кристаллизации, повышению концентрации фторида алюминия в маточных растворах и снижению скорости кристаллизации. [23]
 |
Выходная кривая фронтального анализа. [24] |
Меняя концентрацию исходного раствора, находят количество вещества, адсорбированного при данных условиях. [25]
Определяют концентрацию исходного раствора FeCl2 методом окислительно-восстановительного титрования. В стакан для титрования помещают 2 мл раствора FeCl2, добавляют 10 мл разведенной ( 1: 1) НС1, нагревают раствор на водяной бане до 70 - 80 С и ставят его на магнитную мешалку. Опускают в титруемый раствор платиновый и хлорсеребряный электроды, а также якорь магнитной мешалки, подключают электроды к соответствующим клеммам рН - метра. Установив приблизительно место скачка потенциала, производят точное титрование. С этой целью снова берут 2 мл испытуемого раствора FeCl2 и 10 мл НС1, разбавленной 1: 1, в стакан для титрования, предварительно промытый дистиллированной водой. Перед началом второго точного титрования электроды также промывают водой и осушают их фильтровальной бумагой. После получения скачка потенциала добавляют еще 3 - 4 порции титранта и титрование заканчивают. [26]
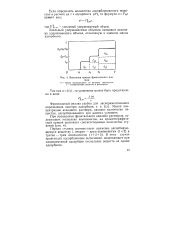 |
Выходная кривая фронтального анализа. [27] |
Меняя концентрацию исходного раствора, находят количество вещества, адсорбированного при данных условиях. [28]
С - концентрация исходного раствора, моль / л; р - содержание стирола, %; 104 1 и 118 2 - молекулярные веса стирола и а-метилстирола. [29]
 |
Диаграмма равновесия фаз процесса. [30] |
Страницы: 1 2 3 4 5