Концентрация - реагент
Cтраница 1
Концентрация реагента в реакционной фазе с определяет при этом как бы неприкосновенный запас реагента. Стоит увеличить скорость реакции - и равновесие (1.3) нарушится. Реакция системы на внешнее воздействие направлена в сторону уменьшения эффекта этого воздействия. [1]
Концентрации реагентов легко установить колориметрированием, если известны концентрации исходных веществ и если одна из солей бесцветна, а вторая окрашена. [2]
Концентрация реагента во всех растворах одинакова - CHR 2 14 IQ-6 M. [3]
Концентрация реагента и ( или) рН слишком низки, поэтому концентрация аниона А реагента в водной фазе недостаточна для образования нейтрального комплекса в преобладающем количестве. В водной фазе в этом случае преимущественно существуют ступенчато образующиеся низшие, положительно заряженные комплексы. [4]
Концентрация реагентов в растворе определяет не только изменение краевого угла, но и его гистерезис. [5]
Концентрация реагента должна быть такой, чтобы условие ( IX, 10) выполнялось по всей колонне. [6]
Концентрации реагентов при химическом равновесии называется равновесными концентрациями. [7]
Концентрация реагента А в точке отбора пробы при установившемся режиме процесса составляет С0 0 6 моль / л; плотность лробы при транспортировании на анализ остается неизменной. [8]
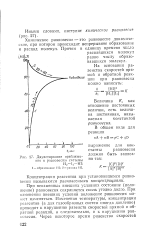 |
Двухстороннее приближение к равновесию системы Н2 - 12 - HI. / - образование HI. 2 -распад HI. [9] |
Концентрации реагентов при установившемся равновесии называются равновесными концентрациями. [10]
Концентрация реагентов при сочетании должна быть подобрана так, чтобы к концу сочетания не допустить чрезмерного загустевания массы и не слишком разбавлять массу, так как это замедляет процесс сочетания. [11]
Концентрация реагента настолько высока, что дезактивация при соударениях реагирующих молекул происходит гораздо чаще, чем диссоциация. В этих условиях устанавливается приблизительно постоянная концентрация возбужденных молекул, поддерживаемая активирующими и дезактивирующими соударениями. Небольшая доля этих возбужденных молекул постоянно реагирует, а их общая концентрация и, следовательно, скорость реакции пропорциональна концентрации реагента в первой степени. [12]
Концентрация реагента настолько низка, что большинство возбужденных молекул успевает прореагировать до столкновения с другой невозбужденной молекулой. [13]
 |
Произведение растворимости бензоилметилдпоксимата никеля. [14] |
Концентрация реагента равна найденной ранее растворимости бензоилметилдиоксима в воде ( 3 77 - 1СГ3 М), так как опыты производили в присутствии твердого реактива. [15]
Страницы: 1 2 3 4