Концентрация - роданид
Cтраница 3
Интенсивность окраски зависит от ряда факторов - кислотности, концентрации роданида и времени стояния. При этой кислотности интенсивность окраски довольно постоянна в течение часа, уменьшаясь лишь немного в течение первых 5 мин. При кислотности выше или ниже указанной окраска слабее, и обесцвечивание раствора наступает быстрее. Ослабление окраски при стоянии особенно заметно в сильнокислых растворах. [31]
На рис. 3 и 4 показана зависимость экстракции комплексов от концентрации роданида и нитрона в водной фазе. [32]
Было найдено18, что состав окрашенных комплексных ионов зависит от концентрации роданида в растворе. При соотношении Со2 1: SCN-1: 1 получается комплексный ион [ Co ( SCN) ], дающий максимум поглощения света при 530 ni ( i. При увеличении концентрации роданид-иона образуются соответственно Co ( SCN) 2 с максимумом поглощения при 570 т [ А, затем [ Co ( SCN) s ] - и [ Co ( SCN) 4 ] 2 - с максимумом поглощения при - 650 mji. Дальнейшее увеличение концентрации роданид-иона не дает заметного смещения максимума, что указывает на отсутствие образования ионов с более высоким числом адден-дов. [33]
На основании этих данных легко установить оптимальные пределы рН, концентраций роданида и нитрона в водной фазе, которые необходимы для максимального извлечения соответствующего комплекса дихлорэтаном. [34]
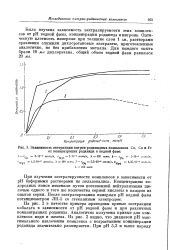 |
Зависимость экстракции нитрон-роданидных комплексов Со, Си и Fe от концентрации роданида в водной фазе. [35] |
Была изучена зависимость экстрагируемости этих комплексов от рН водной фазы, концентрации роданида и нитрона. Оптическую плотность измеряли при толщине слоя 1 см, растворами сравнения служили дихлорэтановые экстракты, приготовленные аналогично, но без прибавления металла. [36]
 |
Оценка стабильности показателей состава сточной воды КХЗ.| Биохимическая очистка сточных вод. [37] |
Поэтому для предприятия, в сточных водах которого исходная концентрация фенолов превышает концентрации роданидов не более чем в 2 - 2 5 раза, целесообразно проводить одноступенчатую очистку, причем время пребывания вод должно определяться условиями разложения роданидов. [38]
Увеличение концентрации хлорида, которое мы обозначим через х, равно уменьшению концентрации роданида. [39]
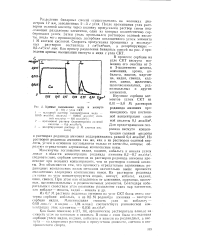 |
Кривые вымывания меди ( 1. 10 с угля СКТ. [40] |
Максимумы поглощения индия, кадмия, кобальта и никеля углем лежат в области концентрации роданида аммония 0 2 - 0 7 мол / дм, следовательно, сорбция элементов из растворов роданида аммония происходит при меньших концентрациях, чем из растворов соляной кислоты. Это объясняется тем, что прочность отрицательно заряженных ро-данидных комплексных ионов металлов значительно выше прочности аналогичных хлоридных комплексных ионов. Из растворов роданида аммония на угле концентрируются индий, висмут, кобальт, кадмий, цинк, свинец. При этом они отделяются от алюминия, марганца, щелочных, щелочноземельных и редкоземельных элементов. [41]
При введении 25 % ацетона половина от общего количества кобальта связывается в комплекс при концентрации роданида в 50 раз меньше, чем в водном растворе. Дальнейшее прибавление ацетона способствует более полному образованию комплекса, хотя оно и менее эффективно. При введении 60 - 75 об. % ацетона необходимая концентрация роданида уменьшается в 110 - 250 раз. На рис. 66 представлены спектры поглощения растворов роданидных комплексов кобальта в 50 % - ном ацетоне при концентрации кобальта 10 - 3 г-моль / л и различном избытке роданида. [42]
Роданиды образуют в кислом растворе с Mov окрашенные соединения, состав которых зависит от концентрации роданида. Ионы MoVI восстанавливают до ионов Mov хлоридом олова ( II), иодидом калия, аскорбиновой кислотой или тиомочевиной в присутствии солей меди ( II) и другими восстановителями. [43]
 |
Абсолютный предел обнаружения элементов различными методами. [44] |
Так, при определении кобальта в виде синего роданидного комплекса необходимо создать очень высокур концентрацию роданида. Несмотря на хорошую растворимость роданида калия, не удается полностью перевести кобальт в комплексное соединение. Тем не менее прибавление ацетона, который хорошо смешивается с водой, приводит к резкому снижению предела обнаружения кобальта из-за возрастания константы устойчивости комплекса. Все эти проблемы детально рассмотрены в разделе фотометрических методов анализа. [45]
Страницы: 1 2 3 4 5