Концентрация - поглощаемое вещество
Cтраница 1
Концентрация Y поглощаемого вещества может быть заменена его парциальным давлением р в паро-газовой смеси. [1]
Уяач - концентрация поглощаемого вещества в газе, поступающем на адсорбцию, кг вещества / кг инертного газа; дог - скорость газовой смеси, отнесенная к полному сечению адсорбера, м / сек ( обычно 0 08ч - 0 25); VCM - расход парогазовой смеси, м / сек. [2]
КОн - концентрация поглощаемого вещества в поглотителе, отнесенная к единице чистого поглотителя. [3]
В результате адсорбции концентрация поглощаемого вещества в потоке уменьшается по мере перемещения его через слой адсорбента. Поэтому и количество ( концентрация) адсорбируемого вещества по высоте слоя адсорбента также изменяется в пределах от максимального до минимального, соответствующего состоянию равновесия с потоком, покидающим слой адсорбента. [4]
В результате адсорбции концентрация поглощаемого вещества в потоке уменьшается по мере перемещения его через слой адсорбента. [5]
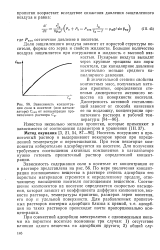 |
Зависимость концентра . [6] |
По мере увеличения концентрации поглощаемого вещества в растворе степень адсорбции его пористым материалом стремится к определенному пределу, отвечающему насыщению носителя поглощаемым веществом. Соотношение компонентов на носителе определяется скоростью насыщения, которая зависит от коэффициента диффузии компонентов, вязкости раствора, температуры пропитки, размеров зерен носителя, его пор и удельной поверхности. Для разбавленных пропиточных растворов изотерма адсорбции близка к прямой, т.е. адсорбция из таких растворов происходит почти пропорционально концентрации. [7]
При протекании процесса адсорбции концентрация поглощаемого вещества ( сорбтива) в адсорбенте непрерывно увеличивается. Это предельное содержание сорбтива в 1 кг ( или в 1 см3) адсорбента, соответствующее полному насыщению адсорбента поглощаемым веществом, называется статической емкостью или статической активностью адсорбента. Статическая емкость зависит от структуры адсорбента, от природы адсорбируемого вещества, его парциального давления ( концентрации) в газовой фазе и от температуры. [8]
При протекании процесса адсорбции концентрация поглощаемого вещества ( адсорбата) в адсорбенте непрерывно увеличивается. В пределе при достижении равновесия между газовой фазой и адсорбентом она достигает наибольшего значения, возможного при данных условиях. [9]
Адсорбционное равновесие зависит от концентрации поглощаемого вещества и температуры. С увеличением концентрации абсолютное число адсорбированных молекул растет. При повышении температуры, наоборот, получает преобладание десорбция. Кроме того, сорбция вещества находится в прямой зависимости от поверхности адсорбента; наибольшей адсорбционной способностью обладают мелкопористые и порошкообразные вещества. [10]
За это же время концентрация поглощаемого вещества в элементе слоя увеличивается на dX и количество вещества, поглощенного слоем высотой dH, составляет SdHQadX, где S - площадь поперечного сечения адсорбента, он-насыпная масса адсорбента. [11]
За это же время концентрация поглощаемого вещества в элементе слоя увеличивается на dX и количество вещества, поглощенного слоем высотой dH, составляет 5 dH p dX, где S - площадь поперечного сечения адсорбента, р - насыпная масса адсорбента. [12]
 |
Выходная кривая ( тпр - время защитного действия слоя. т - время достижения равновесия. [13] |
Для выявления характера распределения концентраций поглощаемого вещества в газовой фазе и в слое адсорбента в данный момент времени необходимо в общем случае составить и решить при соответствующих начальных и граничных условиях систему уравнений материального баланса, изотермы и кинетики адсорбции, гидродинамики процесса. Решение такой системы уравнений возможно лишь путем их упрощения за счет введения ряда допущений и приближений, рассмотрения частных, наиболее простых случаев динамики адсорбции. [14]
Попытки непрерывно регистрировать изменение концентрации поглощаемого вещества в вытекающем растворе, казалось быг заранее обречены на неудачу, так как невозможны без определения с высокой степенью точности разности концентраций в жидкой фазе между входом и выходом измерительной ячейки. В конце-опыта эта разность может составлять 0 1 % и менее от измеряемой величины. В то же время эта трудность в ряде случаев может быть преодолена, если за кинетикой следить по концентрации десорби-рующегося вещества за слоем сорбента. Продемонстрируем сказанное на примере ионного обмена, когда концентрация вытесняемого иона в исходном растворе по крайней мере на три порядка меньше концентрации за сорбентом, и вытесняемый ион не вступает в химическое взаимодействие с другими компонентами в растворе. [15]
Страницы: 1 2 3 4