Концентрация - соль - магний
Cтраница 1
Концентрация солей магния невелика, поэтому их пересчитывают на эквивалентное количество солей кальция. [1]
Изменение концентрации соли магния в растворе влияет как на значение потенциала, отвечающего замедлению спада потенциала ( второй участок кривой), так и на время до резкого смещения потенциала в положительном направлении ( фиг. В более разбавленном растворе MgClz в связи с большим содержанием растворенного кислорода время до достижения защитного потенциала оказывается меньше. [2]
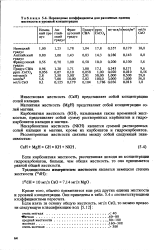 |
Переводные коэффициенты для различных единиц жесткости и уровней концентрации. [3] |
Магнитная жесткость ( MgH) представляет собой концентрацию солей магния. [4]
Проссер [67] показал, что синапсы шестого брюшного ганглия рака обладают низкой чувствительностью к ацетилхолину по сравнению с ганглиями млекопитающих - только при концентрации 6 - 10 - 3 М наблюдалось возбуждение, за которым следовала блокада. Изменение концентрации солей магния и кальция вызывали действие лишь после скрытого периода, продолжавшегося около 30 мин. [5]
Было изучено влияние концентрации ц природы солей магния на результаты и ход титрования. Найдено, что концентрация солей магния в растворе не должна быть меньше 0 6 г-мо. [6]
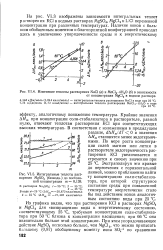 |
Изменение теплоты растворения NaCl ( а и МпС12 - 4Н2О ( б в зависимости.| Интегральные теплоты растворения MgSO4 ( безводн. до постоянной концентрации т 0 139. [7] |
ДЯт становятся менее эндотермич-ными. По мере роста концентрации солей магния или лития в растворителе эндотермичность растворения КС1 увеличивается и стремится к своему значению при 25 С. Экстраполируя эти кривые до пересечения с горизонтальной линией, можно приближенно найти ту концентрацию соли-стабилизатора, при которой структурное состояние среды при повышенной температуре энергетически стало бы под действием ионов аналогичным состоянию воды при 25 С. Из графика видно, что при растворении КС1 в растворах MgSO4 и MgCl2 для возвращения воды к энергетическому состоянию, соответствующему 25 С, требуемая концентрация соли-стабилизатора при 50 С близка к концентрации насыщения; при 66 С она значительно больше этой концентрации. [8]
Крайние значения ДЯШ при концентрации соли-стабилизатора в растворителе, равной нулю, отвечают теплотам растворения КС1 при соответствующих высоких температурах. В соответствии с изложенным в предыдущем разделе, dMIJdT 0 и значения АЯОТ становятся менее эндотермичными. По мере роста концентрации солей магния или лития в растворителе эндотермичность растворения KG1 увеличивается и стремится к своему значению при 25 С. [9]
Как уже было указано, магнезиты встречаются в природе сравнительно редко. Поэтому уже давно проводятся работы по изысканию рационального способа производства чистой гидроокиси магния из природных рассолов магнезиальных солей. Для этой цели особенно подходящими являются соляные озера Крыма и рапа Сивашей, концентрация солей магния в которых более чем в 3 раза превышает концентрацию их в морской воде. [10]
Ценным магниевым сырьем являются ископаемые калиево-маг-ниевые минералы44 - карналлит, каинит, лангбейнит, полигалит и др. ( см. гл. В больших концентрациях сосредоточен Mg2 в рапе Крымских озер, оз. Эльтон, озер Кулундинской степи, в воде Сиваша, Каспийского моря и особенно примыкающего к нему Кара-Богаз - Гола. Концентрация солей магния в рапе озер иногда достигает 30 %, например, в оз. Концентрированный хромагние-вый щелок получается и при переработке карналлита ( см. гл. [11]
Ценным магниевым сырьем являются ископаемые калиево-маг-ниевые минералы44 - карналлит, каинит, лангбейнит, полигалит и др. ( см. гл. В больших концентрациях сосредоточен Mg2 в рапе Крымских озер, оз. Эльтон, озер Кулундинской степи, в воде Сиваша, Каспийского моря и особенно примыкающего к нему Кара-Богаз - Гола. Концентрация солей магния в рапе озер иногда достигает 30 %, например, в оз. Концентрированный хромагние-вый щелок получается и при переработке карналлита ( см. гл. [12]
Крайние значения ДЯШ при концентрации соли-стабилизатора в растворителе, равной нулю, отвечают теплотам растворения КС1 при соответствующих высоких температурах. HJdT 0 и значения М1т становятся менее эндотермичными. По мере роста концентрации солей магния или лития в растворителе эндотермичность растворения КС1 увеличивается и стремится к своему значению при 25 С. [13]
Ценным магниевым сырьем являются ископаемые калиево-магние-вые минералы38 - карналлит, каинит, лангбейнит, полигалит и др. ( см. гл. Морская вода, содержащая - 1 3 г / л Mg2 - практически неисчерпаемый сырьевой источник для производства соединений магния зэ. В больших концентрациях сосредоточен Mg2 в рапе Крымских озер, оз. Эльтон, озер Кулундинской степи, в воде Сиваша, Каспийского моря и особенно примыкающего к нему Кара-Богаз - Гола. Концентрация солей магния в рапе озер иногда достигает 30 %, например в оз. [14]
Страницы: 1