Концентрация - хлористая соль
Cтраница 2
Из уравнения ( 5) можно видеть, что выход по току уменьшается с возрастанием концентрации щелочи Cz и увеличивается с повышением концентрации хлористой соли С. Из этого же уравнения вытекает, что с повышением температуры электролиза выходы должны увеличиваться, так как при низких температурах числа переноса ионов ОН больше, чем числа переноса катиона. [16]
Сущность процесса обессоливания промысловой нефти заключает - ся в снижении кониентраиии хлористых солей в капельной попутной пластовой воде, которая осталась в промысловой нефти после ее предварительного и глубокого обезвоживания. Снижение концентрации хлористых солей в капельной пластовой воде, представляющей собой дисперсную фазу в обратной водонефтяной эмульсии ( промысловой нефти), возможно только в результате коалесиенши их с каплями промывной воды, в качестве которой, как правило, используется пресная вода. [17]
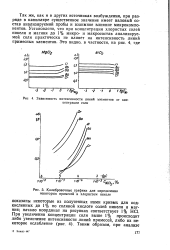 |
Калибровочные графики для определения некоторых примесей в хлористом никеле. [18] |
Так же, как и в других источниках возбуждения, при разряде в капилляре существенное значение имеет валовый состав анализируемой пробы и взаимное влияние микрокомпонентов. Установлено, что при концентрации хлористых солей никеля и магния до 1 % микро - и макросостав анализируемой соли практически не влияет на интенсивность линий примесных элементов. [19]
При электролизе с неподвижным электролитом состав анолита и католита непрерывно изменяется - концентрация хлористой соли уменьшается, анолит насыщается хлором и продуктами его гидролиза, в католите возрастет содержание щелочи. Если вести электролиз без применения специальных мер предосторожности, например диафрагм, то вследствие конвекции и диффузии перемешивание электродных продуктов будет происходить очень быстро и выход по току по хлору и щелочи будет близок к нулю. Конвекция и в значительной мере диффузия устраняются применением диафрагмы. Наличие диафрагмы не препятствует переносу, так как если не будет переноса, то не будет и прохождения тока через электролизер. [20]
С - растворимость газа, г / л; i - плотность тока, а / м2 и Л - постоянная, зависящая от типа электрода и от происходящего на нем процесса. Опыты подачи питающего электролита в хлорные ванны через поры графитового анода показали, что увеличение концентрации хлористой соли, достигаемое таким образом внутри анода, позволяет на 20 - 40 / 6 увеличить его стойкость или, сохраняя нормальное разрушение графита, увеличить степень превращения хлористой соли до 70 - 80 % и соответственно повысить концентрацию щелочи. [21]
Исследование засоленности и загрязнения воздуха в прибрежной зоне района Батуми показало, что скорость коррозии металлов по сезонным циклам связана не только со спецификой метеорологических элементов, но и со степенью засоленности и загрязнения воздуха. Разрушение металлов и металлических покрытий протекает более активно в осенний и зимний периоды в связи с увеличением концентрации хлористых солей и сернистого газа в атмосфере. Количество хлорид-ионов в атмосфере достигает максимальных значений в конце осени, минимальных - во второй половине лета. По сезонным циклам меняется также и содержание в атмосфере сернистого газа, которое в ноябре и декабре составляет 15 - 17 мг / м2 сут. [22]
В первом случае ванну заполняют рассолом и электролиз ведут до получения насыщенного или почти насыщенного раствора хлорноватокислой соли, после чего раствор из ванны сливают и направляют на кристаллизацию. Во время работы в ванну периодически доливают рассол, чтобы пополнить убыль воды от испарения и поддержать концентрацию хлористой соли, которая не должна падать ниже 100 г / л во избежание уменьшения электропроводности раствора. [23]
Исследования касались растворов азотной кислоты ( 300 - 800 г / л) и азотнокислого уранила ( 320 г / л); они показали, что присутствие менее 1 % хлористых солей вызывает коррозию нержавеющей стали ( типа 18 - 8 с добавкой титана) в парах, что было объяснено образованием летучего хлористого нитрозила. В зависимости от условий конденсации паров коррозия могла носить общий характер или быть представлена точечной формой. Свободная кислотность, концентрация хлористых солей, температура и присутствие растворенного кислорода играют важную роль в определении формы коррозии. [24]
Состав фильтрата и воды необходимо знать для оценки целесообразности применения того или иного способа регулирования свойств промывочной жидкости. Это связано с определением химического состава промывочной жидкости, главным образом концентрации минеральных солей. Чаще всего определяют концентрацию хлористых солей и солей, характеризующих жесткость воды. Иногда приходится оценивать химический состав дисперсионной среды после введения веществ с целью изменения тех или иных свойств жидкости. Обычно исследованию подвергается фильтрат, полученный при измерении показателя фильтрации. [25]
При определении массы нетто продукта определяют массу балласта. Для этого измеряют содержание воды и концентрацию хлористых солей в нефти и рассчитывают их массу. Массу механических примесей определяют, принимая среднюю массовую долю их в нефти в соответствии с действующими стандартами, техническими условиями ( ТУ) и другими нормативными документами. [26]
Плотность распределения капель воды по размерам, как показывают экспериментальные исследования, подчиняется логарифмически нормальному закону. Наибольшей вероятностью встречи и слипания обладают капли разного размера, причем чем больше различие размеров, тем больше вероятность коалесценции. Таким образом, для возможности выравнивания концентрации хлористых солей в большей части капельной воды необходимым условием является многократность актов коа-лесиениии и последующего диспергирования капельной воды обрабатываемого в процессе обессоливания сырья. [27]
Страницы: 1 2