Концентрация - сорбтиво
Cтраница 1
Концентрация сорбтива в газе и температура газа одинаковы по сечению слоя. [1]
Затем из-за увеличения концентрации сорбтива в слое происходит постепенное увеличение средней величины адсорбции и, соответственно, уменьшается движущая сила процесса. Это в свою очередь вызывает замедление скорости адсорбции в слое. [2]
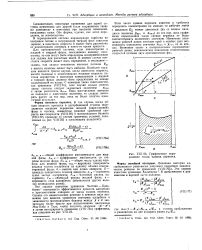 |
Графическое определение числа единиц переноса. [3] |
В периодической системе концентрации сорбтива во входящем потоке и загруженной твердой фазе известны заранее, и константа скорости k может быть рассчитана из концентрации раствора в какое-то время процесса. [4]
 |
Зависимость времени защитного действия от высоты слоя. [5] |
Зона, в которой концентрации сорбтива изменяются от начальных значений до нуля, имеется только в газовой фазе. [6]
При протекании процесса адсорбции концентрация сорбтива в адсорбенте непрерывно увеличивается. В пределе при достижении равновесия между паро-газовой фазой и адсорбентом она достигает наибольшего значения, возможного при данных условиях. Это предельное содержание сорбтива в 1 кг ( или в 1 еж3) адсорбента, соответствующее полному насыщению адсорбента поглощаемым веществом, называется статической емкостью ( стати ческой активностью) адсорбента. Статическая емкость зависит от структуры адсорбента, от природы адсорбируемого вещества, его парциального давления в газовой фазе ( концентрации), от температуры. [7]
СР - средняя по высоте слоя концентрация сорбтива в газе. [8]
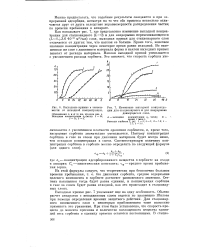 |
Выходные кривые в зависимости от исходной концентрации.| Изменение выходной концентрации для стационарного и для непрерывно движущегося слоя. [9] |
Степень насыщения тогда будет равна единице, и концентрация сорбтива в газе за слоем будет равна исходной, как это происходит в стационарных слоях. [10]
Уравнения ( VIII-61) и ( VI II - 62) вместе с соответствующими уравнениями скорости ( и, если необходимо, - равновесия) приводят к вычислению концентрации сорбтива в твердой и жидкой фазах в зависимости от времени. Например, по зависимости скорости реакции уравнение ( VIII-48), которое имеет очень широкую применимость, результирующий интеграл аналогичен интегралу, приведенному Хоу-геном и Ватсоном 2 для однородных обратимых реакций 2-го порядка. [11]
Особенностью уравнений неизотермической кинетики сорбции для обеих моделей является их существенная нелинейность в силу нелинейности термического уравнения сорбции а / ( с, Т) и зависимости в общем случае входящих в указанные уравнения параметров переноса от концентрации сорбтива и температуры. В связи с этим к настоящему времени обе модели изучены в неизотермическом случае совершенно недостаточно. [12]
Функция hw ( t ], описывающая приращение выходной концентрации сорбтива в газе, имеет несколько другой вид. Затем из-за увеличения концентрации сорбтива в слое происходит постепенное увеличение средней величины адсорбции и, соответственно, уменьшается движущая сила процесса. Это в свою очередь вызывает замедление скорости адсорбции в слое. [13]
Как уже отмечалось выше, наряду с предположением об идеальном перемешивании газа в плотной фазе псевдоожиженного слоя нередко используется предположение об идеальном вытеснении газа в плотной фазе слоя. В этом случае математическую модель процесса адсорбции в псевдоожиженном слое следует видоизменить. Уравнение ( 6.6 - 2) для определения профиля концентрации сорбтива в газовых пузырях останется тем же самым. [14]
Однако сходство изотермы защитного действия ингибиторов с изотермой адсорбции проявляется лишь в зоне малых концентраций ингибиторов ( стр. Добавление в корро-зионно-активную среду больших количеств ингибиторов приводит, как правило, к увеличению скорости растворения металла ( см. рис. 5, стр. В соответствии с адсорбционной теорией защитного действия ингибиторов это возрастание коррозии должно быть связано с десорбцией ингибитора. Однако не известно случаев, когда увеличение концентрации сорбтива ( в известных пределах, порядка м-моль 1л) приводило бы к десорбции. [15]
Страницы: 1 2