Концентрация - сульфид-ион
Cтраница 3
Растворимость сульфидов металлов увеличивается с уменьшением концентрации сульфид-иона. Концентрацию сульфид-ионов можно понизить, связывая сульфид-ионы в мало диссоциированную сероводородную кислоту, путем образования тио-ионов амфотерных элементов и изменяя степень окисления серы. Для расчета растворимости сульфидов металлов следует пользоваться условным произведением растворимости ( гл. [31]
Кислота подавляет диссоциацию H2S, уменьшая концентрацию сульфид-иона в 100 раз по сравнению с дистиллированной водой. [32]
В результате создаются условия, при которых концентрация сульфид-ионов постепенно становится такой, что произведение концентраций катионов четвертой и пятой групп и сульфид-иона становится больше их произведений растворимости, и сульфиды металлов этих групп выпадают в осадок. Катионы третьей аналитической группы при рН С 1 5 в осадок не выпадают, так как произведения растворимости сульфидов третьей группы являются значительно большими величинами, чем произведения растворимости сульфидов четвертой и пятой групп. [33]
В результате создаются условия, при которых концентрация сульфид-ионов становится такой, что произведение концентраций катионов IV и V групп и сульфид-иона оказывается больше их произведений растворимости, и сульфиды металлов этих групп выпадают в осадок. Катионы III аналитической группы при рН 1 5 не осаждаются, так как произведения растворимости сульфидов III группы являются значительно большими величинами, чем произведения растворимости сульфидов IV и V групп. [34]
В 1 М растворе ( NH4) 2S концентрация сульфид-ионов fS - l - 10-с г-ион / л и рН - 9 26 ( см. гл. S - - ] в щелочном растворе чрезвычайно возрастает. [35]
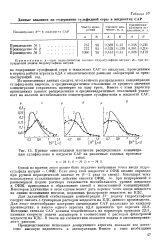 |
Данные анализов на содержание сульфидной серы в жидкостях САР.| Кривые относительной плотности распределения концентрации сульфид-иона в жидкости САР на различных содовых производ. [36] |
Из приведенных данных следует, что плотность распределения концентрации сульфид-иона выросла, а среднеквадратичное отклонение от среднего значения концентрации сократилось примерно на одну треть. Вместе с этим характер приведенных кривых распределения и среднеквадратичных отклонений указывает на наличие нестабильности концентрации сульфид-иона в жидкости САР. [37]
Осаждение малорастворимых сульфидов зависит от их про изведения растворимости и концентрации сульфид-ионов в вод -, ном растворе. [38]
Последнее соотношение указывает, что при постоянной концентрации недиссоциированных молекул сероводорода концентрация сульфид-ионов изменяется обратно пропорционально квадрату концентрации водородных ионов. [39]
Максимум флуоресценции наблюдается при Х530 нм, пропорциональность между тушением и концентрацией сульфид-иона сохраняется в пределах 0 001 - 0 02 мкг / мл S при концентрации тетрамеркурацетатфлуоресцеина 0 8 мкг / мл. [40]
По мере увеличения [ Н можно достичь такого состояния, при котором концентрация сульфид-ионов уменьшится до таких пределов, когда сульфиды IV группы будут выпадать в осадок, а осаждение сульфидов III группы наблюдаться не будет. [41]
Максимум флуоресценции наблюдается при К 530 нм, пропорциональность между тушением и концентрацией сульфид-иона сохраняется в пределах 0 001 - 0 02 мкг / мл S при концентрации тетрамеркурацетатфлуоресцеина 0 8 мкг / мл. [42]
По мере увеличения [ Н ] можно достичь такого состояния, при котором концентрация сульфид-ионов уменьшится до таких пределов, когда сульфиды IV группы будут выпадать в осадок а осаждение сульфидов III группы наблюдаться не будет. [43]
При определении сульфид-ионов возможны ошибки измерения, вызванные присутствием ионов водорода, которые влияют на концентрацию свободных сульфид-ионов в растворе. Во всех растворах, кроме сильнощелочных, сульфид-ион образует с ионами водорода гидросульфид или сероводород. В этом случае концентрацию сульфид-ионов можно найти расчетным путем, используя данные о равновесии системы водород-сульфид-ион, полученные методом потенциометрического титрования раствором нитрата серебра. [44]
Чтобы отделить сульфиды катионов четвертой группы от катионов третьей группы, необходимо создать в растворе такую концентрацию сульфид-иона, которая была бы достаточна для осаждения катионов четвертой и пятой групп и недостаточна для осаждения катионов третьей группы. Такую концентрацию S2 можно создать, поддерживая определенную концентрацию ионов Н, так как от последней зависит концентрация S2 - ( стр. [45]
Страницы: 1 2 3 4