Концентрация - окисленная форма
Cтраница 1
Концентрация окисленной формы у поверхности капли, когда достигнута точка Б, практически уменьшается до нуля. Для всех значений потенциала после точки Б она изчезающе мала. [1]
Если концентрация окисленной формы в 100 раз больше концентрации восстановленной формы, потенциал превышает реальный стандартный потенциал на величину ( 0 059 / z) Ig 100 0 12 / 2 вольт. [2]
Если концентрация окисленной формы в 100 раз больше концентрации восстановленной формы, потенциал превышает реальный стандартный потенциал на ( 0 059 / г) lg 100 0 12 / г В. [3]
Уменьшение концентрации окисленной формы при постоянной концентрации восстановленной снижает потенциал исследуемой системы, и наоборот, всякое уменьшение концентрации восстановленной формы при постоянной концентрации окисленной увеличивает окислительно-восстановительный потенциал. Так, например, введение в раствор, содержащий ферри - и ферроионы, ацетата натрия уменьшает окислительно-восстановительный потенциал, так как ионы трехвалентного железа связываются в комплекс. Введение в эту же систему оксалата аммония, образующего комплекс с железом ( II), увеличивает потенциал изучаемой системы. [4]
Уменьшение концентрации окисленной формы при постоянной концентрации восстановленной снижает потенциал исследуемой системы, и наоборот, всякое уменьшение концентрации восстановленной формы при постоянной концентрации окисленной увеличивает окислительно-восстановительный потенциал. Так, например, введение в раствор, содержащий ферри-и ферроионы, ацетата натрия уменьшает окислительно-восстановительный потенциал, так как ионы трехвалентного железа связываются в комплекс. Введение в эту же систему оксалата аммония, образующего комплекс с железом ( II), увеличивает потенциал изучаемой системы. [5]
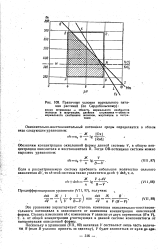 |
Граничные условия нормального пита. [6] |
Обозначим концентрацию окисленной формы данной системы К. [7]
Обозначим концентрацию окисленной формы данной системы, V, а общую концентрацию окислителя и восстановителя В. [8]
При этом концентрация окисленной формы вещества вблизи поверхности электрода уменьшится, а концентрация восстановленной формы увеличится. [9]
При этом концентрация окисленной формы ионов УЗ значительно меньше восстановленной формы J -, поэтому при отсутствии внешнего воздействия на мембраны у катода создается запорный слой и через прибор проходит только небольшой ток покоя, обусловленный естественной конвекцией ионов / з к катоду. [10]
Если обозначить концентрацию окисленной формы иона через [ Окисл. [11]
ОХ ] - концентрация окисленной формы ионов; [ Red ] - концентрация восстановленной формы ионов; Z - - число электронов, участвующих в реакции; Е0 - нормальный потенциал. [12]
Во втором случае концентрация окисленной формы компонента системы повысится с соответствующие понижением концентрации восстановленной формы компонента этой системы. [13]
Через некоторое время в результате электролиза концентрация окисленной формы приближается к нулю. Из уравнения (2.26) следует, что в таком случае потенциал электрода должен достигать очень больших отрицательных значений. На практике потенциал электрода резко меняется и достигает потенциала основного электролита или другого вещества в растворе, способного восстанавливаться при более положительных потенциалах, чем потенциалы разложения основного электролита. [14]
С увеличением плотности катодного тока ] концентрация окисленной формы у поверхности электрода со уменьшается, что приводит к увеличению результирующей скорости превращения Y в О. Последняя достигнет наибольшей величины при CQ О, и дальнейшее увеличение плотности катодного тока в рамках механизма (3.60) окажется невозможным. [15]
Страницы: 1 2 3 4