Концентрация - фторид-ион
Cтраница 2
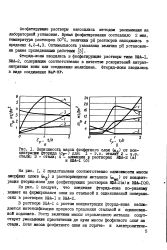 |
Зависимость массы фосфатного слоя 6в. ь от концентрации фторида ( Ср - для. I - г. о. сталит 2 - э.о. стали. 3 - стали. 4 - алюминия в растворах КФА-2 ( а. [16] |
В растворе КФА-I с ростом концентрации фторид-иона наблюдается интенсификация процесса травления стальной и оцинкованной подложек. Росту величины массы стравленного металла сопутствует уменьшение практически до нуля массы фосфатного слоя на стали. [17]
Приготовляют серию стандартных растворов с концентрациями фторид-ионов от 0 до 2 50 мг / л, разбавляя дистиллированной водой соответствующие объемы рабочего стандартного раствора. Затем вносят в каждый раствор реактивы, как описано в ходе анализа, через 1 ч измеряют оптические плотности и строят график зависимости оптической плотности от концентрации. [18]
Приготовляют серию стандартных растворов с концентрациями фторид-ионов от 0 до 2 50 мг / л, разбавляя дистиллированной шодой соответствующие объемы рабочего стандартного раствора. Затем вносят в каждый раствор реактивы, как описано в ходе анализа, через 1 ч измеряют оптические плотности и строят график зависимости оптической плотности от концентрации. [19]
Электродная функция линейна в рабочем диапазоне концентраций фторид-ионов 10 - 5 - 10 - 4 г-ион / л, или 0 02 - 0 2 мг F - в 100 мл раствора, наклон прямой составляет 58 1 мВ / декада. [20]
Наносят на график по оси абсцисс концентрацию фторид-иона в мг / л, а по оси ординат оптическую плотность ( показания барабана), соединяя полученные точки, строят калибровочную кривую. [21]
Вес образца должен быть таков, чтобы концентрация фторид-иона была от 0 1 до 0 3 мг на 1 мл конечного раствора. Образец смешивают с 200 мг высушенного порошка сахара ( аналитический реактив), добавляют около 4 г перекиси натрия, иногда к смеси добавляют 200 мг перхлората натрия в качестве катализатора. Озоление образца выполняют обычным образом. В случае если образец жидкий, его взвешивают в желатинной капсуле, которую затем погружают в смесь сахара и перекиси натрия, суммарный вес которых равен 200 мг, включая капсулу. [22]
Типичный калибровочный график, используемый для определения концентрации фторид-ионов. [23]
После введения аликвотной части анализируемого раствора определяют концентрацию свободных фторид-ионов и затем прибавляют избыток твердого карбоната аммония. Далее вновь определяют концентрацию фторид-ионов и содержание урана в анализируемом растворе рассчитывают по разности результатов двух измерений. [24]
Однако необходимо иметь в виду, что повышение концентрации фторид-ионов часто приводит к образованию комплексов с большим координационным числом, которые сравнительно хорошо растворяются в воде. [25]
Он допустим в концентрациях, не превышающих / з концентрации фторид-ионов. При большем его содержании, а также в присутствии бора и при анализе вод сложного и неизвестного состава рекомендуется проводить отгонку, описанную в разд. Анализ обычных вод этим методом такой отгонки не требует. [26]
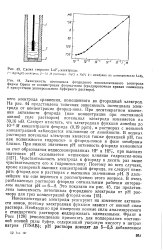
На рис. 44 представлена типичная зависимость потенциала электрода от концентрации фторид-иона. Следует отметить, что электродная функция линейна до 10 - 5 М концентрации фторида ( 0 19 ррт), в растворах с меньшей концентрацией наблюдается отклонение от линейности. В водных растворах потенциал электрода является также функцией рН, так как подвижности гидроксил - и фторид-ионов в фазе мембраны близки. [28]
Следовательно, образование разнолигандного комплексд происходит в определенных пределах концентраций фторид-иона. Этот факт был учтен в дальнейшем. [29]
По стандартным растворам строят калибровочную кривую и по ней определяют концентрацию фторид-ионов в исследуемой воде. [30]
Страницы: 1 2 3 4