Концентрация - цирконий
Cтраница 3
В описанных условиях проведения реакции ее чувствительность составляет 0 05 мкг циркония в 10 мл раствора, линейная зависимость между концентрацией циркония и интенсивностью флуоресценции раствора сохраняется вплоть до 30 мкг циркония в 10 мл раствора. [31]
 |
Растворимость гидроокисей циркония и гафния в растворах едкого натра. [32] |
Результаты этого исследования 467 ] проливают свет на большой разнобой в вопросе о форме ионов циркония в растворе: достаточно небольшого изменения концентрации циркония или кислотности раствора, чтобы изменилась и форма существования иона циркония. [33]
Для покрытия способам катафореза применяются составы, которые в отличие от используемых при изготовлении анодов характеризуются пониженной ( в 2 раза) концентрацией циркония ( табл. 9 - 9), чем обеспечиваются большая равномерность слоя и отсутствие местных утолщений на витках. [34]
Цилен и Конник [817] повторили работы предыдущих авторов и подтвердили, что в 1 и 2 М НС1О4 при 25 С в интервале концентраций циркония 10 - 4 - 10 - 2 М основными формами являются тример и тетрамер циркония. [35]
Изучая влияние концентрации циркония на его поглощение катионитом КУ-1 из хлорнокислых растворов, Бабко и Набивансц [31] подтвердили, что фактор полимеризации возрастает при увеличении концентрации циркония и уменьшении кислотности среды. Относительная, скорость диализа ионов циркония одинакова в растворах хлорной, соляной и азотной кислот при равных условиях. Отсюда можно сделать вывод, что на фактор полимеризации в растворах не влияют хлорид - и нитрат-ионы. При действии фторида, оксалата, перекиси водорода, ацетил ацетона полимерные формы циркония разрушаются. Авторы установили также, что основная масса циркония в растворе находится не в виде смеси полимерных ионов, а в виде одной формы в зависимости от концентрации циркония и кислотности раствора. [36]
 |
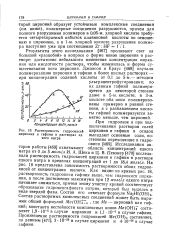
Зависимость фактора полимеризации ионов циркония от концентрации и рН раствора. Цифры на прямых соответствуют величине фактора полимеризации. [37] |
Состав полимера, иначе говоря фактор полимеризации, не зависит от природы аниона кислоты ( исследования проводились в соляно -, хлор-но - и азотнокислых растворах), но зависит от концентрации циркония и от рН раствора. [38]
 |
Электролитическая ячейка. [39] |
Видно, что, если потенциал металлического циркония остается постоянным во время опыта и по величине близок к значениям, приводимым в работе [3], то потенциал висмутового электрода в присутствии металлического циркония постепенно возрастает, причем тем быстрее, чем больше концентрация циркония в электролите. [40]
Центрифугируют и переливают раствор в склянку. Концентрация циркония в этом растворе составляет примерно 1 мг / мл. [41]
К исследуемому раствору ( контрольная задача) в колбе вместимостью 25 мл добавляют 1 мл раствора морина и разбавляют до метки 2М соляной кислотой. Концентрацию циркония в исследуемом растворе определяют по градуировочному графику. [42]
Раствором сравнения служит аналогичный раствор, но без циркония. Концентрацию циркония находят по калибровочному графику, для построения которого в делительные воронки отбирают стандартные растворы циркония ( от 2 до 150 мкг) в 10 мл 11 N НС1 и каждую порцию экстрагируют 7 5 мл 0 1 М три-н-октиламина. В мерные колбы емкостью 50 мл отбирают по 5 мл органического экстракта, прибавляют те же. [43]
Через Г5 мин измеряют интенсивность флуоресценции. Концентрацию циркония в исследуемом растворе определяют по градуировочному графику. [45]
Страницы: 1 2 3 4
