Концентрация - жидкий гидрат
Cтраница 1
Концентрации жидких гидратов не являются произвольными. Соответствующий метод был впервые указан в книге Ван-дер - Ваальса и Констамма [ 19, стр. [1]
Концентрация жидкого гидрата NT не является произвольной, а примет, согласно принципу равновесия [ 12, стр. [2]
С ростом общей концентрации раствора концентрации жидких гидратов возрастают все медленнее и, как видно из рис. 2, при достаточно больших концентрациях раствора становятся практически постоянными величинами. По этой причине кривые Н / ( УС) с ростом концентрации раствора постепенно выпрямляются. [3]
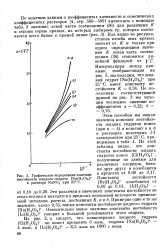 |
Графическое определение констант. [4] |
Из рис. 2, а следует, что концентрация жидкого гидрата [ С1 ( Н20) 4 ] - не может превысить 6 моль, гидрата [ Na ( H20) 4 ] - 4 моль, a [ Li ( H20) 4 ] - 8 5 моль на 1000 г воды. [5]
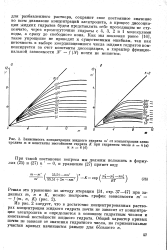 |
Зависимость концентрации жидкого гидрата т от концентрации электролита т и константы нестойкости гидрата К при гидратном числе п 4 ( а. [6] |
Из рис. 2 следует, что в достаточно концентрированных растворах концентрация жидкого гидрата почти не зависит от концентрации электролита и определяется в основном гидратным числом и константой нестойкости жидкого гидрата. [7]
С помощью уравнения ( 19) легко построить диаграмму зависимости NT f ( N) концентрации жидкого гидрата от концентрации электролита в растворе. Такая диаграмма для п 4 изображена на рис. 1 в виде серии изолиний, каждая из которых отвечает определенному значению константы нестойкости К. Из этой диаграммы наглядно видно, что с ростом концентрации раствора концентрация жидкого гидрата сначала пропорционально увеличивается, потом рост ее замедляется, и в крепких растворах концентрация жидкого гидрата остается практически постоянной, не зависящей от моляль-ности раствора. [8]
К сожалению, определяемые экспериментальным путем коэффициенты активности и избыточные термодинамические свойства раствора характеризуют суммарный эффект взаимодействия частиц раствора, разделить который на три части, соответствующие трем слагаемым формулы ( 5), не представляется возможным без опытных данных о составе и концентрации жидких гидратов ионов, об объемных и тепловых эффектах, связанных с их образованием в растворе. Отсутствие этих данных является, на наш взгляд, основной причиной, мешающей дальнейшему прогрессу теории растворов электролитов. [9]
Гидратная теория растворов электролитов [1] обобщена на смешанные растворы двух солей с общим ионом. Выведена формула для свободной энтальпии раствора и активности электролита и дан метод расчета концентрации жидких гидратов ионов и кривых растворимости солей в тройных растворах по опытным данным об активности электролита в водном растворе каждой из этих солей в отдельности. [10]
Если исходить из концепции жидких гидратов как комплексных соединений, способных к диссоциации, и принять, как показано нами [17], что константа нестойкости К достаточно большая величина, порядка 10-а - 10 - г, то из рис. 1 видно, что всегда какая-то часть воды окажется свободной. Границу полной сольватации следует понимать, по нашему мнению, как ту концентрацию раствора, при которой происходит излом на кривых рис. 1 и концентрация жидких гидратов в растворе достигает устойчивого максимума. [11]
С помощью уравнения ( 19) легко построить диаграмму зависимости NT f ( N) концентрации жидкого гидрата от концентрации электролита в растворе. Такая диаграмма для п 4 изображена на рис. 1 в виде серии изолиний, каждая из которых отвечает определенному значению константы нестойкости К. Из этой диаграммы наглядно видно, что с ростом концентрации раствора концентрация жидкого гидрата сначала пропорционально увеличивается, потом рост ее замедляется, и в крепких растворах концентрация жидкого гидрата остается практически постоянной, не зависящей от моляль-ности раствора. [12]
С помощью уравнения ( 19) легко построить диаграмму зависимости NT f ( N) концентрации жидкого гидрата от концентрации электролита в растворе. Такая диаграмма для п 4 изображена на рис. 1 в виде серии изолиний, каждая из которых отвечает определенному значению константы нестойкости К. Из этой диаграммы наглядно видно, что с ростом концентрации раствора концентрация жидкого гидрата сначала пропорционально увеличивается, потом рост ее замедляется, и в крепких растворах концентрация жидкого гидрата остается практически постоянной, не зависящей от моляль-ности раствора. [13]
Страницы: 1