Концентрация - гидроксид - натрий
Cтраница 3
На основании полученных данных строят на одном графике кинетические кривые изменения степени гидролиза полиакриламида для четырех опытов, проведенных при различных концентрациях гидролизующего агента. Затем находят логарифмы v и концентрации гидроксида натрия. [31]
Из этого следует, что при нормальном механизме МФК не следует ожидать простой линейной зависимости от концентрации катализатора. Изменения в скорости реакции, полученные при варьировании концентрации гидроксида натрия в водной фазе и добавления в-нее бромида, также не согласовывались с предположением о том, что эти изменения связаны с простой экстракцией гидроксида четвертичного аммония в органическую фазу. Хотя общее уравнение кинетики реакции вывести не удалось, полученные данные лучше всего соответствуют механизму, рассмотренному выше. [32]
Растворы илидов можно получать и в двухфазных системах, так как сами фосфониевые соли являются катализаторами фазового переноса. В качестве органических растворителей обычно выбирают бензол или дихлорметан [25]; наибольшие выходы достигаются путем варьирования концентрации гидроксида натрия в водной фазе. [33]
При получении вискозы гидратированные ионы Na и НО проникают и в аморфные и в кристаллические области ксантогената целлюлозы, в результате чего разрушается надмолекулярная структура и происходит растворение. Растворимость ксантогената целлюлозы зависит от степени замещения, степени полимеризации, степени однородности ксантогената по химическому составу, температуры, концентрации гидроксида натрия в растворе. С увеличением СП ксантогената растворимость его снижается и ухудшается фильтруемость вискозы. Этим и обусловливается необходимость предсозревания щелочной целлюлозы. [34]
Ниже на рис. 18 приведены графические зависимости скорости гидролиза и-ксилилендихлорида от концентрации гидроксида натрия. Из приведенных данных видно, что скорость реакции гидролиза п-ксилилендихло-рида как в водно-спиртовой, так и в водной средах в сильной степени зависит от концентрации гидроксида натрия. При гидролизе п-ксилилен-дихлорида в водном растворе гидроксида натрия реакция протекает по первому порядку. В процессе реакции меняется лишь концентрация щелочного агента, хлорид же мало растворим в воде и находится в избытке; его концентрация в растворе поддерживается практически постоянной. В водной среде, но в отсутствие гидроксида натрия, порядок реакции нулевой. [35]
Продолжительность щелочения определяет размеры башни. Большинство башен щелочения рассчитаны на 60 - 90 минут. Концентрация гидроксида натрия снижается на протяжении всей обработки, и для полного потребления данного химиката продолжительность обработки должна быть не менее 60 минут. [36]
Буферные добавки предназначены для поддержания рН раствора на оптимальном уровне. В качестве таковых используют соли уксусной, лимонной, гликолевой и других кислот. При повышении концентрации гидроксида натрия с 20 до 60 г / л скорость осаждения покрытия увеличивается. Добавление в этом случае стабилизирующей добавки ( нитрат таллия) способствует сохранению оптимального значения рН и оптимальной концентрации восстановителя. [37]
В процессе выпаривания по мере роста концентрации гидроксида натрия растворимость хлорида натрия снижается и начинается выпадение твердой соли из раствора. На рис. 3.15 показана зависимость растворимости хлорида натрия от концентрации гидроксида. Быстрое снижение растворимости происходит до концентрации гидроксида натрия 400 кг / м3, причем при этом выпадает чистая соль, не загрязненная присутствующим в растворе сульфатом натрия. [38]
Основным фактором, влияющим на процесс нейтрализации масла, является концентрация рабочего раствора гидрокида натрия. С ростом концентрации раствора NaOH увеличивается степень омыления нейтрального жира, повышается общее содержание жира в соапстоке, снижается выход нейтрального жира. В то же время с ростом концентрации гидроксида натрия увеличивается адсорбционная способность образующегося соапстока, следовательно, улучшается очистка масла. Наиболее важными показателями процесса нейтрализации являются кислотное числа рафинированного масла и содержание мыла в масле после нейтрализации. Такие показатели являются функцией отклика в данной работе. [39]
В качестве таких добавок следует использовать жидкие маловязкие вещества, хорошо растворимые в обеих фазах эмульсии. Например, при периодическом автоматическом контроле концентрации гидроксида натрия в водном соле-щелочном растворе, составляющем дисперсную фазу устойчивой эмульсии продуктов синтеза эпоксидной смолы ( дисперсионная среда), в эмульсию добавляют толуол, который резко снижает вязкость и плотность дисперсионной среды. Скорость гравитационного разделения фаз такой дестабилизированной эмульсии резко возрастает, уже через 3 - 4 мин после введения толуола можно отделять осветленную водную фазу и направлять ее на анализ. Скорость расслоения водной эмульсии эпоксидной смолы в значительной степени определяется количеством добавляемого растворителя и температурой. [40]
Раствор 1 используют при температуре от 80 до 100 С, поднимая ее по мере его эксплуатации до верхнего предела. Продолжительность обработки увеличивают при этом от 5 до 20 мин. Отклонение от оптимальных значений температуры раствора и концентрации гидроксида натрия сопровождается ухудшением качества покрытия - чрезмерное повышение их приводит к формированию рыхлой оксидной пленки, а понижение - к получению пленок небольшой толщины. [41]
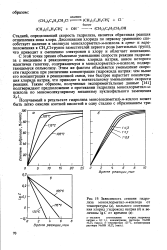 |
Зависимость степени гидролиза монохлорметил-м-ксилола от температуры ( а, мольного соотношения хлорид. гидроксид натрия ( б и величины IgC от времени ( в. [42] |
Стадией, определяющей скорость гидролиза, является обратимая реакция отщепления иона хлора. Диссоциации хлорида по первому уравнению способствует наличие в молекуле монохлорметил-л-ксилола в орто - и пара-положениях к СН2С1 - группе заместителей первого рода ( метальных групп), что приводит к смещению электронов к хлору и облегчает ионизацию. Этим же фактом объясняется уменьшение скорости гидролиза при увеличении концентрации гидроксида натрия: чем выше его концентрация в реакционной смеси, тем быстрее нарастает концентрация хлорида натрия, что приводит к значительному уменьшению скорости реакции. [43]
 |
Влияние условий окисления антрацена на выход продуктов и со. [44] |
Кроме фталевой кислоты, в больших количествах образуются. Соотношение между ними колеблется в широких пределах в зависимости от условий окисления. Термоокислительная стабильность 2 3-нафталнндикарбоновой кислоты снижается при повышении температуры, уменьшении концентрации гидроксида натрия и продолжительности окисления. [45]
Страницы: 1 2 3 4