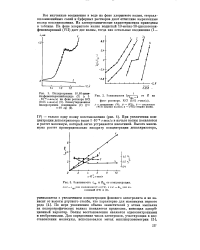
Концентрация - деполяризатор
Cтраница 2
Поэтому концентрация деполяризатора в объеме раствора практически не уменьшается при электролизе, и если объем исследуемого раствора не слишком мал, то кривую можно снимать несколько раз, не меняя раствора, и все полученные кривые будут идентичны. Если применять тонко оттянутый капилляр, то электролиз можно изучать, используя небольшие объемы раствора ( 0 01 - 0 005 мл), что очень важно для применения полярографии в микроанализе; здесь, однако, при повторении электролиза уже необходимо учитывать, что концентрация деполяризатора в растворе уменьшается. [16]
Предел концентрации деполяризатора, до которого ход кривой титрования отвечает уравнению 1КС, зависит от размера индикаторного электрода. [17]
При этой концентрации деполяризатора анодные и катодные кривые пересекаются при потенциале 0 2 б и отпущенная сталь корродирует с небольшой скоростью. Требуется значительное время, пока в растворе накопятся продукты коррозии, которые сместят потенциал в отрицательную сторону до 0 1 в, при котором уже наблюдается усиленная межкристаллитная коррозия. [18]
С - концентрация деполяризатора; а - коэффициент переноса; Я, - потенциал электрода при протекании тока. [19]
С увеличением концентрации деполяризатора высота предволны стремится к пределу, отвечающему полному заполнению поверхности электрода тормозящей пленкой, суммарный же предельный ток предволны и основной волны подчиняется уравнению Ильковича. Примером образования псевдопредволн при торможении электродного процесса являются анодные волны, при которых продукт электрохимической реакции взаимодействует со ртутью, образуя нерастворимую пленку. [20]
При увеличении концентрации деполяризатора адсорбционный пик смещается в направлении положительных потенциалов и уменьшается по сравнению с пиком диффузионного тока. [21]
При увеличении концентрации деполяризатора и периода капания ЕЧ, первой волны становится положительнее, что отвечает обратимому или квазиобратимому процессу с последующей химической реакцией 2-го порядка ( см. гл. После макроэлектролиза при потенциале плато первой волны выделены дифенилсульфид и дифенилртуть; электролиз при потенциалах, соответствующих площадке второй волны, дал дифенилсульфид и бензол. [22]
При увеличении концентрации деполяризатора выше 1 - 10 - г-мол / л в начале волны появляется и растет максимум, который легко устраняется желатиной. [24]
Таким образом, концентрация деполяризатора в растворе остается неизменной и в то же время поверхность капли ртути на катоде периодически обновляется. [25]
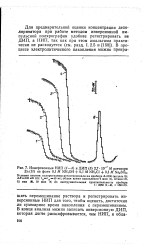 |
Инверсионные НИП ( 1 - 4 и ДИП ( 5 2 7 10 - 7 М раствора Zn ( II на фоне 0 1 М NH4OH 0 1 М МН4С1 0 1 М NaaSO8. [26] |
Для предварительной оценки концентрации деполяризатора при работе методом инверсионной импульсной полярографии удобнее регистрировать не ДИП, а НИП, так как при этом амальгама практически не расходуется ( см. разд. [27]
Если с ростом концентрации исходного деполяризатора, а следовательно и парамагнитной частицы, наблюдается уширение линий СТС спектра ЭПР, то анализ такой зависимости позволяет изучить сверхбыстрые реакции с участием радикальных частиц ( значения констант скорости бимолекулярного взаимодействия лежат в пределах 106 - 109 л / молъ-сек), например перенос электрона между ион-радикалом и исходной молекулой ( реакция электронного обмена) в зависимости от природы растворителя или другие гомогенные процессы, уменьшающие время жизни радикальной частицы и вызывающие уширение линий СТС. [28]
Переходное время зависит от концентрации деполяризатора и силы тока, проходящего через электролитическую ячейку: чем больше концентрация деполяризатора и меньше сила тока, тем больше переходное время при прочих равных условиях, и наоборот. [29]
Как общее правило, концентрация деполяризатора не влияет на природу продукта восстановления, хотя она и может оказать влияние на выход по току при восстановлении. Всякий фактор, который облегчает доступ деполяризатора к катоду, увеличивает подъем кривой ( рис. 120), изображающей зависимость плотности тока от потенциала катода. [30]
Страницы: 1 2 3 4 5