Примерная концентрация
Cтраница 2
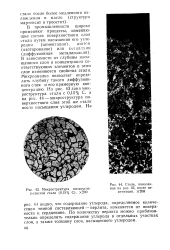 |
Микроструктура низкоуглеродистой стали ( 0 15 % С. Х200.| Сталь, показанная на 42, после цементации. Х200. [16] |
В зависимости от глубины насыщенного слоя и концентрации соответствующих элементов в этом слое изменяются свойства стали. Микроанализ позволяет определить глубину такого диффузионного слоя и его примерную концентрацию. На рис. 43 дана микроструктура стали с 0 15 % С, а на рис. 44 - микроструктура поверхностного слоя этой же стали после насыщения углеродом. [17]
 |
Кривые поглощения света раствором соединения, полученного при взаимодействии никеля с диметилглиоксимом. [18] |
Измеряют значение оптической плотности полученного раствора и при помощи калибровочного графика определяют концентрацию меди в миллиграммах на 100 мл раствора. Если раствор содержит больше 12 мг меди в 100 мл и известна его примерная концентрация, то раствор разбавляют водой в мерной колбе с таким расчетом, чтобы он содержал от 3 до 12 мг меди в 100 мл. [19]
На практике наибольшее распространение нашли борфто-ридные и n - фенолсульфоновые электролиты, Относительные концентрации свинца и олова в растворе выбирают в зависимости от состава сплава. Для получения сплава с малым содержанием олова ( 8 - 12 %) примерные концентрации солей составляют 120 - 160 г / л Pb ( BF4) 2 и 25 - 35 г / л Sn ( BF4) 2; для сплавов, содержащих 60 2 % олова ( эвтектический сплаз), электролит имеет состав: 5 - 25 г / л Pb ( BF4) 2 и 20 - 60 г / л Sn ( BF4) 2, 100 - 350 г / л свободной борфтористоводородной кислоты и 20 - 30 г / л борной кислоты. Температура электролитов 18 - 30 С; аноды - комбинированные ( из олова и свинца) или из сплава, соответствующего составу катодного осадка. [20]
В качестве рабочих растворов используют чаще всего растворы кислот хлороводородной и серной, растворы гидроксидов NaOH и КОН. Поскольку эти кислоты и гидроксиды не могут быть использованы как исходные вещества для приготовления титрованных растворов, то сначала готовят растворы примерной концентрации, а точный титр и нормальную концентрацию их устанавливают по исходным веществам. [21]
В качестве рабочих растворов испо льзуют чаще всего растворы кислот соляной и серной, растворы гидроксидов NaOH и КОН. Поскольку эти кислоты и гидроксиды не могут быть использованы как исходные вещества для приготовления титрованных растворов, то сначала готовят растворы примерной концентрации, а точный титр и нормальность их устанавливают по исходным веществам. [22]
Таким образом, при условии малой зависимости кривой экстракции от кислотности раствора типа амина и концентрации металла при помощи величин ступенчатой константы диссоциации можно рассчитать концентрацию ад денда 50 % - ной экстракции, а затем примерную концентрацию 100 % - ной экстракции металла. Для применяемых нами условий найдено, что кривые экстракции хлоридных комплексов цинка и висмута мало зависят от кислотности раствора и концентрации металла. То же самое наблюдается и при экстракции хлоридных комплексов висмута. Это связано с тем, что вначале при увеличении концентрации аддендов образуются однозарядные ацидокомплексы, и кривые экстракции их разными аминами близки. При увеличении концентрации аддендов образуются более сложные ацидокомплексы. [23]
Удовлетворительная воспроизводимость и высокая точность результатов при количественном определении аминокислот могут быть достигнуты только при условии снятия показателей с одной и той же хроматограммы, характеризующих стандартную и исследуемую смеси аминокислот. Смеси метчиков готовят из такого расчета, чтобы концентрация каждой отдельной аминокислоты в смеси наиболее близко соответствовала концентрации данной аминокислоты в испытуемом растворе. Если примерная концентрация свободных аминокислот в исследуемых образцах растений неизвестна, то предварительно хроматографируют испытуемые образцы и по этим данным готовят смеси известных аминокислот - метчиков. Смеси метчиков составляют так, чтобы все аминокислоты в смесях хорошо отделялись одна от другой. [24]
На практике наибольшее распространение нашли борфто-ридные и n - фенолсульфоновые электролиты. Относительные концентрации свинца и олова в растворе выбирают в зависимости от состава сплава. Для получения сплава с малым содержанием олова ( 8 - 12 %) примерные концентрации солей составляют 120 - 160 г / л Pb ( BF4) 2 и: 25 - 35 г / л Sn ( BF4) 2; для сплавов, содержащих 60 2 % олова ( эвтектический сплав), электролит имеет состав: 5 - 25 г / л Pb ( BF4) 2 и 20 - 60 г / л Sn ( BF4) 2, 100 - 350 г / л свободной борфтористоводородной кислоты и 20 - 30 г / л борной кислоты. Температура электролитов 18 - 30 С; аноды - комбинированные ( из олова и свинца) или из сплава, соответствующего составу катодного осадка. [25]
Таким образом, коагуляция происходит при концентрации каучука вдвое меньше исходной. В момент разведения водой коагуляция останавливается, так как концентрация электролита-коагулянта падает в несколько сот раз и становится весьма малой, т, определенная с помощью нефелометра, характеризует систему в момент разведения взятой из нее пробы. Примерные концентрации электролитов указаны на стр. [26]
В момент разведения водой коагуляция останавливается, так как концентрация электролита-коагулянта падает в несколько сот раз и становится весьма малой, т, определенная с помощью нефелометра, характеризует систему в момент разведения взятой из нее пробы. Опыт прекращают, когда - с начинает падать. Примерные концентрации электролитов указаны на стр. [27]
Исходные исследуемые растворы имеются в лаборатории. Химическим анализом определены их концентрации. Концентрации растворов в разных бутылях несколько различаются, поэтому вместе с концентрацией взятого раствора записывайте номер бутыли. Ниже в описании дается примерная концентрация используемых растворов, но все расчеты проводите с концентрациями, указанными на этикетках бутылей. [28]
По некоторым данным рекомендуется в конце процесса, когда гидролиз прошел на 70 - 80 %, частично разбавить раствор с целью более полного выделения титана в осадок; обычно постепенно добавляют 35 - 40 % воды по отношению к начальному объему раствора. Общая длительность операции гидролиза 6 - 8 час. Зародыши, применяемые в этом процессе, представляют собою коллоидный раствор гидрата окиси титана и получаются неполной нейтрализацией раствора сернокислого титана. Нейтрализация производится путем медленного добавления в раствор сернокислого титана раствора щелочи с примерной концентрацией 100 г / л NaOH. При добавлении щелочи выпадает белый хлопьевидный осадок, который вначале переходит в раствор быстро, затем медленнее с образованием мути и, наконец, желатинируется. При быстром охлаждении и энергичном размешивании масса вновь становится жидкой. [29]
Классический макрометод химического анализа связан с большими затратами времени и средств и, кроме того, со значительным расходом реактивов. Оборудование дорого стоит и требует много места, а обильные осадки зачастую являются причиной неточной работы. Полумикрометод анализа лишен недостатков макро - и микрометодов. В полумикрометоде используют сравнительно простое оборудование, техникой метода легко овладеть. Жидкости в основном дозируют по каплям. Так как объем капли зависит от поверхностного натяжения, величина которого примерно одинакова для воды и разбавленных растворов, по каплям можно дозировать равные объемы. Это дает возможность проводить полуколичественные определения и постоянно знать примерную концентрацию иона в добавляемом растворе. [30]
Страницы: 1 2