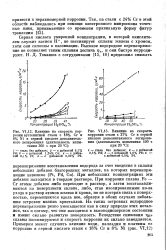
Умеренная концентрация
Cтраница 2
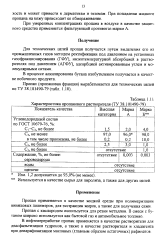 |
Характеристика пропанового растворителя ( ТУ 490 - 79. [16] |
При умеренных концентрациях пропана в воздухе в качестве защитного средства применяется фильтрующий противогаз марки А. [17]
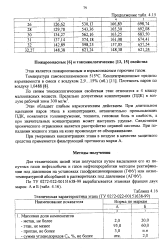 |
Техническая характеристика этана ( ТУ 0272 - 022 - 00151638 - 99. [18] |
При умеренных концентрациях этана в воздухе в качестве защитного средства применяется фильтрующий противогаз марки А. [19]
 |
Строение эмульсий типа масло - вода ( а и вода - масло ( б. [20] |
При умеренных концентрациях воды ( до 10 %) ее влияние на важнейшие показатели качества топлива незначительно. Однако при концентрации воды свыше 20 % значительно повышается теплота испарения, изменяется фракционный состав, в частности повышаются температуры начала кипения и 50 % - го отгона, снижается давление насыщенных паров и скорость испарения. В целом это ведет к ухудшению пусковых свойств и показателей работы двигателя, особенно в период прогрева и при работе на переходных режимах. [21]
В растворах умеренных концентраций степень гидролиза при комнатной температуре невелика. [22]
Серная кисл-ота умеренной концентрации, в которой окислителем служит катион Н, не пассивирует сплавы железа с хромом, хотя они склонны к пассивации. Высокое водородное перенапряжение не позволяет таким сплавам достичь ф, и они быстро корродируют. [24]
В области умеренных концентраций для многих электролитов оправдывается закон кубического корня. Этот закон не вытекает из теории Онзагера, но легко выводится, как следствие теории Гхоша. [25]
В области умеренных концентраций эти формулы находятся в качественном согласии с опытом. Однако предпосылки теории Гхоша не согласуются с современными данными о строении растворов и многие ее выводы противоречат опытным фактам. Так, например, из нее следует, что потенциальная энергия раствора зависит от температуры лишь в той степени, какая отвечает изменению диэлектрической постоянной раствора. В действительности же потенциальная энергия раствора зависит непосредственно от температуры. Результаты рентгеновских и других методов исследования структуры растворов не подтверждают мысли Гхоша о сохранении в растворах электролитов кристаллической решетки исходных соединений. Противоречия между теорией Гхоша и опытом следует отнести в первую очередь за счет того, что в теории не учитывается роль теплового движения, которое в растворах должно нарушать упорядоченное расположение ионов, подобное их расположению в кристалле. [26]
В области умеренных концентраций эти формулы находятся в качественном согласии с опытом. Однако предпосылки теории Гхоша не согласуются с современными данными о строении растворов и многие ее выводы противоречат опытным фактам. Так, например, из нее следует, что потенциальная энергия раствора зависит от температуры лишь в той степени, какая отвечает изменению диэлектрической постоянной раствора. В действительности же потенциальная энергия раствора зависит непосредственно от температуры. Результаты рентгеновских и других методов исследования структуры растворов не подтверждают мысли Гхоша о сохранении в растворах электролитов кристаллической решетки исходных соединений. Противоречия между теорией Гхоша и опытом следует отнести в первую, очередь за счет того, что в теории не учитывается роль теплового движения, которое в растворах должно нарушать упорядоченное расположение ионов, подобное их расположению в кристалле. [27]
В растворах умеренных концентраций степень гидролиза при комнатной температуре невелика. [28]
В области умеренных концентраций эти формулы находятся в качественном согласии с опытом. Однако предпосылки теории Гхоша не согласуются с современными данными о строении растворов и многие ее выводы противоречат опыту. Так, например, из нее следует, что потенциальная энергия раствора зависит от температуры лишь в той степени, какая отвечает изменению диэлектрической проницаемости раствора. В действительности же потенциальная энергия раствора зависит непосредственно от температуры. Результаты рентгеновских и других методов исследования структуры растворов не подтверждают мысли Гхоша о сохранении в растворах электролитов кристаллической решетки исходных соединений. Противоречия между теорией Гхоша и опытом следует отнести, в первую очередь за счет того, что в ней не учитывается роль теплового движения, которое в растворах должно нарушать упорядоченное расположение ионов, подобное их расположению в кристалле. [29]
В растворах умеренных концентраций наиболее склонны к образованию контактных ионных пар слабо гидратирующийся катион и практически любой не гидратирующийся анион. [30]
Страницы: 1 2 3 4