Малая концентрация
Cтраница 1
Малые концентрации выражают в миллимолях ( ммоль) или микромолях ( мкмоль) вещества, содержащихся в 1 л раствора. По тем же соображениям лучше выражать концентрации тольков долях моля ( или грамм-эквивалента), содержащихся в 1 л раствора. Для технических целей концентрации выражают в процентах. [1]
Малые концентрации часто называют следами. Нет определенных данных о конкретных концентрациях, которые следует считать следами. [2]
Малые концентрации до определенного критического значения увеличивают интенсивность коррозии, большие ее уменьшают до весьма малых значений. При 5 - Ю-2 моль / л коррозия полностью прекращается. NaCl 70 мг / л NaaSCu) требуются совсем малые концентрации ингибитора ( 200 мг / л), чтобы полностью подавить коррозионный процесс. Если сравнивать защитные концентрации различных ингибиторов, то для молибдата они наименьшие. [3]
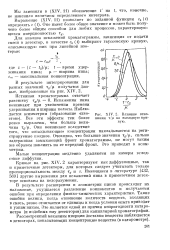 |
Влияние отношения т / ц па выходную кривую. [4] |
Малые концентрации медленно удаляются из камеры вследствие диффузии. [5]
Малые концентрации двух последних частиц повышают растворимость менее, чем на 2 %, Все другие вероятные частицы находятся в пренебрежимо малой концентрации. [6]
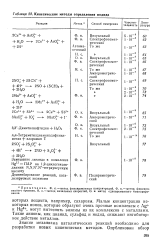 |
Кинетические методы определения иодида. [7] |
Малые концентрации некоторых ионов, которые образуют очень прочные комплексы с Ag и Hg2, могут вытеснять энзимы из их комплексов с металлами. Такие анионы, как цианид, сульфид и иодид, снижают ингибитор-ное действие металлов. [8]
Малая концентрация этих элементов затрудняет определение строения соединений, в состав которых входят эти элементы. [9]
Малые концентрации ( до 1 м-экв) вызывают повышение скорости фильтрации, далее следует понижение скорости фильтрации, затем значительное повышение и, наконец, при наивысших применявшихся нами концентрациях кислоты - вновь падение. Здесь следует указать, что Аррепиус [1], исследовавший влияние рН на скорость осаждения суспензии каолина, пришел к подобным же результатам. Аррениус пытается объяснить полученные им результаты наличием у каолинов изоэлектрической точки. Однако поставленные нами катафо-ретические опыты с достаточною ясностью показали, что и при очень высокой концентрации Н - ионыне в состоянии перезарядить частички каолина. Мы убеждены в том, что вряд ли столь странный ход кривой может быть объяснен с чисто физико-химической точки зрения. Вероятно, здесь сказывается химическое действие кислоты на каолин, осложняющее также влияние Н - ионов на заряд и устойчивость каолинов. [10]
 |
Схема отгонки фенолов из подсмольной воды при помощи пара. [11] |
Малые концентрации в подсмольной воде летучих с паром фенолов приводят к необходимости применять избыток щелочи, иначе легко гидролизирую-щиеся феноляты выделяют фенолы и последние начинают отгоняться с паром. [12]
Малая концентрация этих элементов и отсутствие методов их концентрации затрудняет определение и делает практически невозможной идентификацию соединений, в состав которых они входят. [13]
Малые концентрации фосфатов не стимулируют язвенную коррозию. [14]
Малая концентрация СОг в воздухе ( примерно до 1 %) не токсична, при возрастании ее до 4 - 5 % отмечается сильное раздражение органов дыхания, а при 10 % возможно сильное отравление. [15]
Страницы: 1 2 3 4