Начальная концентрация - исходный реагент
Cтраница 1
Начальные концентрации исходных реагентов Бри исследовании кинетики реакции студент выбирает самостоятельно. Описанная методика позволяет проводить опыты как в избытке спирта, так и при соизмеримых начальных концентрациях кислоты ( ангидрида) и спирта в исходной реакционной смеси. При обработке результатов кинетического эксперимента следует учитывать содержание воды при использовании в качестве исходных реагентов пеаСсолиотированиых спиртов. [1]
ОАО - начальная концентрация исходного реагента Л; ХА - степень превращения по реагенту А; Е, Е2 - энергии активации соответственно для прямой - и обратной реакций; k0i, & о2 - предэкспоненциальные множители констант скоростей прямой и обратной реакций; R - универсальная газовая постоянная; Т - абсолютная температура. [2]
САО - начальная концентрация исходного реагента А; ХА - степень превращения по реагенту А; Е, Е2 - энергии активации соответственно для прямой и обратной реакций; AOI, &02 - пред-экспоненциальные множители констант скоростей прямой и обратной реакций; R - универсальная газовая постоянная; Т - абсолютная температура. [3]
Изменение температуры в политермическом реакторе определяется величиной и знаком теплового эффекта реакции, начальной концентрацией основного исходного реагента, степенью превращения и количеством теплоты, которое подводится в зону реакции или отводится от нее. Изменение температуры рассчитывается по уравнениям теплового баланса реактора, которые учитывают приход теплоты с реагентами, теплоту реакции, теплообмен с окружающей средойчи вынос теплоты с продуктами реакции. [4]
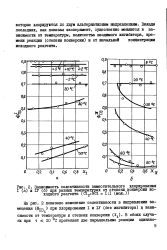 |
Зависимость селективности заместительного хлорирования I ( а и 1У ( б при разных температурах от степени конверсии исходного реагента ( ci2. Rci ( мол. [5] |
Вклады последних, как показал эксперимент, существенно меняются в зависимости от температуры, количества вводимого ингибитора, времени реакции ( степени конверсии) и от начальной концентрации исходного реагента. [6]
 |
Зависимость селективности ф от приведенной степени превращения ХА при хлорировании 1 2-дихлорэтана. [7] |
Если отношение констант скоростей обеих реакций является постоянным или, если энергии активации реакций равны или близки друг к другу, тангенс угла наклона линии, соединяющей на графике обе точки, будет равен отношению энергии активации к универсальной газовой постоянной ( если энергии активации реакций отличаются друг от друга значительно, скорость одной из реакций будет пренебрежимо мала по сравнению со скоростью другой, вследствие чего сложную реакцию можно будет рассматривать как простую), а отрезок, отсекаемый на оси ординат - безразмерному комплексу, включающему предэкспоненциальный множитель, начальную концентрацию исходного реагента и постоянные а и b уравнения гиперболы. [8]
Если отношение констант скоростей обеих реакций является постоянным или, если энергии активации реакций равны или близки друг к другу, тангенс угла наклона линии, соединяющей на графике обе точки, будет равен отношению энергии активации к универсальной газовой постоянной ( если энергии активации реакций отличаются друг от друга значительно, скорость одной из реакций будет пренебрежимо мала по сравнению со скоростью другой, вследствие чего сложную реакцию можно будет рассматривать как простую), а отрезок, отсекаемый на оси ординат - безразмерному комплексу, включающему, предэкспоненциальный множитель, начальную концентрацию исходного реагента, и постоянные а и & уравнения гиперболы. [9]
Для первой по ходу газа псевдосекции степень превращения z / i определяется по уравнениям для аппаратов полного смешения при заданных начальной концентрации исходных реагентов у, константе скорости реакции k и времени контакта взаимодействующих реагентов в одной ячейке TI. Степень превращения во второй псевдосекции у2 определяется по тем же уравнениям для аппаратов полного смешения, а величина концентрации исходных реагентов на входе во вторую псевдосекцию определяется разностью Уп-У - В такой последовательности определяется степень превращения для третьей, четвертой и так далее до п псевдосекции. [10]
Например, в простейшем случае двух последовательных необратимых реакций, в которых кинетика получения основного продукта В описывается уравнением 2-го порядка, а побочного продукта D - уравнением 1-го порядка, соотношение количеств В и D растет пропорционально начальной концентрации исходного реагента А. Соответственно увеличивается и избирательность. [11]
Страницы: 1