Начальная концентрация - вещество
Cтраница 2
С ] - начальная концентрация вещества в том растворителе, из которого растворенное вещество подвергается экстракции, г / л; ХУд - удельный коэффициент распределения; v - объем второго растворителя, л на 1 л и первого растворителя. [16]
Через С обозначаются начальные концентрации веществ и ионов в растворе, выраженные, так же как и равновесные концентрации, в молях на литр и, соответственно, в грамм-ионах на литр раствора. [17]
Через С обозначаются начальные концентрации веществ в растворе, выраженные, так же как и равновесные концентрации, в молях на литр. В растворе сильного электролита концентрация иона равна или в целое число раз больше концентрации растворенного вещества, выраженной в молях на литр. [18]
Обозначим: а - начальная концентрация вещества А, Ъ - начальная концентрация вещества В; с - начальная концентрация вещества С; х - количество прореагировавших исходных веществ или, что то же, количество образующихся конечных продуктов за время т ( минуты, секунды) от начала реакции; k - константа скорости, которая для данной реакции при данных условиях является величиной постоянной. [19]
АО и В0 - начальные концентрации веществ А и В, ж - убыль концентраций А и В, и равно концентрации образовавшегося продукта. [20]
АО, Ап - начальная концентрация вещества А и равновесная концентрация самоассоциата, выраженные в мольных долях. [21]
Пусть ui и а2 - начальные концентрации веществ А и Л2; х - число прореагировавших к моменту t молей вещества А, а следовательно, и вещества Az, так как каждый моль вещества Л4 соединяется с молем вещества Л2, и поэтому число прореагировавших молей обоих веществ одинаково. [22]
А, молей; Ь - начальная концентрация вещества В, молей; х - содержание каждого исходного вещества в образующемся продукте, молей; т - время, мин. [23]
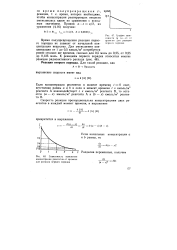 |
График зависимости lg ( a - х от времени для реакции первого порядка.| Зависимость изменения концентрации реагентов от времени для реакции первого порядка. [24] |
Время полупревращения реакции первого порядка не зависит от начальной концентрации вещества. Для уменьшения концентрации от 1 до 0 5 кмоль / м3 потребуется ровно столько же времени, сколько для 0 5 моль до 0 25, от 0 25 др 0 125 моль. [25]
Величина т50у для реакции первого порядка пе зависит от начальной концентрации вещества. И в разбавленном и в концентрированном растворе половина вещества распадается за одинаковый промежуток времени. [26]
Это уравнение представляет собой модель, количественно описывающую влияние начальной концентрации вещества X, продолжительности реакции и ее температуры на количество получаемого вещества Y при постоянной температуре. [27]
Для упрощения расчетов эксперимент обычно проводят при условии, что начальная концентрация вещества в объеме мембраны равна нулю и что вещество диффундирует через мембрану в объем почти с нулевой концентрацией. [28]
Следовательно, период полураспада у реакций второго порядка зависит от начальной концентрации веществ. [29]
Обозначим: а - начальная концентрация вещества А, Ъ - начальная концентрация вещества В; с - начальная концентрация вещества С; х - количество прореагировавших исходных веществ или, что то же, количество образующихся конечных продуктов за время т ( минуты, секунды) от начала реакции; k - константа скорости, которая для данной реакции при данных условиях является величиной постоянной. [30]
Страницы: 1 2 3 4