Мольная концентрация - компонент
Cтраница 4
Нелинейные блоки 5 и 6 обеспечивают воспроизведение выражения A B / V. Сумматор 3 вычисляет текущее значение объема V, а масштабный блок 2 - начальную мольную концентрацию компонента А. [46]
Определение разности между температурами кипения, специально приготовленных эталонных смесей позволяет быстро оценить эффективность разделяющего агента. Для этого смешивают в равных объемах каждый из разделяемых компонентов с предполагаемым разделяющим агентом и опытным путем определяют температуры кипения обеих полученных смесей. Затем эти температуры вычисляют, исходя из мольных концентраций компонентов, при этом предполагают линейную зависимость температуры от состава. Наконец, вычисляют разность температур кипения полученных смесей, при этом используют как экспериментальные, так и расчетные значения температур кипения. [47]
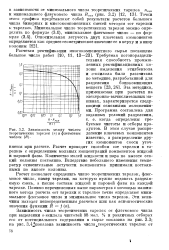 |
Зависимость между числом теоретических тарелок ( п и флегмовым числом ( R. [48] |
Эта методика, применяемая при расчетах на электронно-вычислительных машинах, характеризуется следующими основными положениями. В этом случае распределение ключевых компонентов известно, а распределение других компонентов смеси уточняется при расчете. Расчет проводят сцособом от тарелки к тарелке с определением мольных концентраций компонентов жидкой и паровой фазы. [49]
Актив - ность представляет собой вспомогательную расчетную термодинамическую функцию, которая в суммарной форме характеризует степень связанности молекул компонента. При образовании данным компонентом в растворе каких-нибудь соединений его активность становится меньше и, наоборот, активность возрастает при уменьшении степени ассоциации компонента. Активность дает возможность судить об отклонении свойств данного компонента в том или ином растворе от свойств в простейшем растворе при той же мольной концентрации компонента. Активность зависит от вида и концентрации каждого из других компонентов раствора. Она зависит также от температуры и от давления, но не зависит от способа выражения концентрации и, как показывает равенство ( IX, 23), является величиной безразмерной. [50]
Активность представляет собой вспомогательную расчетную термодинамическую функцию, которая в суммарной формг характеризует степень связанности молекул компонента. При образовании данным компонентом в растворе каких-нибудь соединений его активность становится меньше и, наоборот, активность возрастает при уменьшении степени ассоциации компонента. Активность дает возможность судить об отклонении свойств данного компонента в том или ином растворе от свойств в простейшем растворе при той же мольной концентрации компонента. Активность зависит от вида и концентрации каждого из других компонентов раствора. [51]
Активность представляет собой вспомогательную расчетную термодинамическую функцию, которая в суммарной форме характеризует степень связанности молекул компонента. При образовании данным компонентом в растворе каких-нибудь соединений его активность становится меньше и, наоборот, активность возрастает при уменьшении степени ассоциации компонента. Активность дает возможность судить об отклонении свойств данного компонента в том или ином растворе от свойств в простейшем растворе при той же мольной концентрации компонента. Активность зависит от вида и концентрации каждого из других компонентов раствора. Она зависит также от температуры и от давления, но не зависит от способа выражения концентрации и, как показывает равенство ( IX, 23), является величиной безразмерной. [52]
Это далеко не тривиальный результат химической термодинамики, который стал ясным только после появления теоремы Нернста. Проведение точных расчетов связано с необходимостью знать зависимость летучести от давления ( тогда Кр может не оставаться величиной постоянной при Т const) или активности от мольных концентраций компонентов, когда постоянной является величина Ка, но не Кх. Однако это - общая проблема описания свойств вещества в рамках химической - термодинамики, а не отдельная задача из теории химического равновесия, и если для любых химически неизменных растворов найдены летучести или активности, их можно использовать при расчете химических равновесий. [53]
Существует два источника ошибки: использование приближенных соотношений для расчета вириальных коэффициентов и неадекватность аналитической формы уравнения Вильсона, предлагаемой для расчета коэффициентов активности неконденсирующихся компонентов. В первом случае определение больших значений концентраций малолетучего компонента по малым концентрациям этого компонента в паровой фазе чрезвычайно чувствительно к величине второго вириального коэффициента. Во втором случае большие отклонения от идеальности жидкой фазы могут неадекватно оцениваться при большой летучести компонентов. В результате этого мольные концентрации компонентов жидкой фазы оказываются неоправданно заниженными, поэтому не может быть получено, физически реализуемое давление, которое увеличило бы сумму концентраций до единицы. Оказывается, что при увеличении давления SUMX в конечном счете проходит через максимум вследствие быстрого уменьшения коэффициента фугитив-ности малолетучего компонента. В программе предусмотрен контроль на случай подобной ситуации для того, чтобы прекратить дальнейшие расчеты и вывести наилучшее возможное приближение. [54]
Существует два источника ошибки: использование приближенных соотношений для расчета вириальных коэффициентов и неадекватность аналитической формы уравнения Вильсона, предлагаемой для расчета коэффициентов активности неконденсирующихся компонентов. В первом случае определение больших значений концентраций малолетучего компонента по малым концентрациям этого компонента в паровой фазе чрезвычайно чувствительно к величине второго вириального коэффициента. Во втором случае большие отклонения от идеальности жидкой фазы могут неадекватно оцениваться при большой летучести компонентов. В результате этого - мольные концентрации компонентов жидкой фазы оказываются неоправданно заниженными, поэтому не может быть получено физически реализуемое давление, которое увеличило бы сумму концентраций до единицы. Оказывается, что при увеличении давления SUMX в конечном счете проходит через максимум вследствие быстрого уменьшения коэффициента фугитив-ности малолетучего компонента. В программе предусмотрен контроль на случай подобной ситуации для того, чтобы прекратить дальнейшие расчеты и вывести наилучшее возможное приближение. [55]
Рассмотрим сферическую жидкую каплю в безграничной газовой среде. Жидкая фаза представляет собой раствор, состоящий из инигибитора - водного раствора метанола. Обозначим мольные доли воды и метанола в капле через xw и хм. Газовая фаза представляет собой многокомпонентную смесь, включающую природный газ с мольными концентрациями компонентов у, а также пары воды - ук и метанола ум. В начальный момент времени t 0 заданы радиус капли R0, температуры капли TLO и Тсо, мольные концентрации жидкой хк, хш и газовой уш, уа ] 0, уш фаз. [56]
Благодаря тому, что уравнения ( VII, 6) - ( VII, 9) содержат все основные сведения о химическом равновесии, которые может дать термодинамика, их можно назвать основными уравнениями химической термодинамики. Это далеко не тривиальный результат химической термодинамики, который стал ясным только после появления теоремы Нернста. Проведение точных расчетов связано с необходимостью знать зависимость летучести от давления ( тогда КР может не оставаться величиной постоянной при Т const) или активности от мольных концентраций компонентов, когда постоянной является величина Ка, но не Кх. Однако это - общая проблема описания свойств вещества в рамках химической термодинамики, а не отдельная задача из теории, химического равновесия, и если для любых химически неизменных растворов найдены летучести или активности, их можно использовать при расчете химических равновесий. [57]
Страницы: 1 2 3 4