Средняя концентрация - радикал
Cтраница 1
 |
Структура трека быстрого электрона в конденсированной фазе. [1] |
Средняя концентрация радикалов и других парамагнитных частиц, образующихся в твердой матрице в результате облучения, равна GD, где D - поглощенная доза излучения в эв / г. Эта концентрация может быть определена непосредственно методом ЭПР. Однако радикалы, как будет показано ниже, часто распределены в облучаемом веществе неравномерно. [2]
В другой модификации метода вращающегося сектора измеряется средняя концентрация радикалов в зависимости от скорости вращения диска с секторными прорезями. [3]
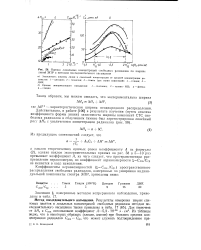 |
Оценка локальных концентраций свободных радикалов по ширине линий ЭПР и методом последовательного насыщения. [4] |
Зависимость ширины линии и локальной концентрации от средней концентрации радикалов: / - цитидин; 2 - гуанизин; 3 -тимин ( две серии измерений) - 4 - глицин - 5 - ДНК. [5]
Зависимость параметра / i / / от расстояния между радикалами приведена на рис. XI.8. Для систем с равномерным распределением радикалов ( стеклующиеся жидкости и аморфные полимеры) зависимости / 1 / 7 от концентрации радикала совпадают, а для систем с неравномерным распределением радикалов ( например, кристаллические полимеры) - не совпадают; при одинаковых средних концентрациях радикалов 1 1 значительно больше, чем для систем с равномерным распределением. [6]
Одним из существенных параметров, определяющих кинетику радикальных реакций в облученных органических веществах, является распределение радикалов в веществе, которое может быть в принципе равномерным или неравномерным. Неравномерность распределения радикалов в облученных образцах, возможно, связана с тем, что радикалы преимущественно образуются и стабилизируются на поверхности или з некоторых выделенных участках объема твердого тела, вблизи дефектов примесей или в треках. При изменении средней концентрации радикалов или при изменении внешних - условий характер распределения радикалов может не сохраниться. [7]
В принципе он основан на том, что при действии света на фотосенсиби-лизированную полимеризацию ( или другую цепную реакцию) скорость, с которой достигается стационарная концентрация радикалов, определяется скоростью квадратичного обрыва цепей. С другой стороны, скорость поглощения мономера зависит от первой степени концентрации радикалов. В результате скорость поглощения мономера может быть прямой мерой средней концентрации радикалов. [8]
Дальнейшая судьба окклюдированных радикалов зависит от физич. В среде осадителя растущие радикалы сворачиваются в достаточно плотные клубки, и активный конец радикала оказывается спрятанным внутри клубка. Кроме того, клубки коагулируют, образуя осадок полимерной фазы. Это приводит к увеличению как средней концентрации радикалов в системе, так и в особенности их концентрации в частицах полимера. Обрыв цепи происходит либо в результате взаимодействия застрявших радикалов с более подвижными радикалами, приходящими из объема жидкой фазы, либо в результате полного захоронения застрявших радикалов в массе полимора. Наблюдаемое часто повышение порядка реакции инициирования по сравнению с гомогенной полимеризацией в жидкой фазе указывает на преобладание второго механизма. Скорость роста цепи с участием окклюдированных радикалов также несколько замедляется вследствие замедленной диффузии мономера внутрь полимерных клубков. Но этот эффект, как правило, перекрывается значительно большим снижением скорости обрыва цепей. Поэтому общая скорость реакции при переходе от гомофазной к гетерофазной полимеризации обычно возрастает. При очень малых скоростях диффузии мо-номера реакция может остановиться полностью. [9]
Дальнейшая судьба окклюдированных радикалов зависит от физич. В среде осадителя растущие радикалы сворачиваются в достаточно плотные клубки, и активный конец радикала оказывается спрятанным внутри клубка. Кроме того, клубки коагулируют, образуя осадок полимерной фазы. Это приводит к увеличению как средней концентрации радикалов в системе, так и в особенности их концентрации в частицах полимера. Обрыв цепи происходит либо в результате взаимодействия застрявших радикалов с более подвижными радикалами, приходящими из объема жидкой фазы, либо в результате полного захоронения застрявших радикалов в массе полимера. Наблюдаемое часто повышение порядка реакции инициирования по сравнению с гомогенной полимеризацией в жидкой фазе указывает на преобладание второго механизма. Скорость роста цепи с участием окклюдированных радикалов также несколько замедляется вследствие замедленной диффузии мономера внутрь полимерных клубков. Но этот эффект, как правило, перекрывается значительно большим снижением скорости обрыва цепей. Поэтому общая скорость реакции при переходе от гомофазной к гетерофазной полимеризации обычно возрастает. При очень малых скоростях диффузии мо-иомера реакция может остановиться полностью. [10]
При 20 арильный радикал реагирует со вторым радикалом примерно с 10s - 104 раз большим выводом столкновений, чем с молекулой толуола в растворителе. Таким образом, в том случае, когда образование бензил-толуола становится важным, концентрация бензильного радикала должна быть порядка 10 - 2 моль. Для создания этой высокой концентрации радикалов необходима очень высокая локальная интенсивность дозы. Это означает, что только некоторые из шпор содержат бензильный радикал и что реже встречаются шпоры больше чем с одним радикалом. Можно оценить средний объем шпор, в которых отдельные радикалы создают среднюю концентрацию радикалов, равную 10 - 2 моль. [11]
Видно, что появляется дополнительное слагаемое ( Та) 1, которое может быть связано со спин-решеточной релаксацией или взаимодействием радикалов с магнитными ядрами окружающих молекул. Изучение ( ТЦ) может также давать полезную информацию о радикалах, в частности, об их структуре. Однако в данном разделе этот вопрос не обсуждается. Второе слагаемое в формуле ( 3) обусловлено диполь-дипольным взаимодействием радикалов. Сравнение экспериментальной ( 7) и теоретической ( 5, 6) зависимостей показывает, что ( С) пропорционально плок в большинстве экспериментов, проведенных как с помощью стационарных методов, так и методом спинового эха. Линейная зависимость величины ( Гв) - г от средней концентрации радикалов проще всего может быть понята, если считать, что распределение радикалов равномерное по всему образцу. Во всяком случае это не соответствует тому, что можно ожидать для трековой модели распределения радикалов. Если бы радикалы стабилизировались в треках и их накопление происходило за счет увеличения числа треков при неизменной локальной концентрации радикалов в треках, то ( Гв) 1 не должно было бы зависеть от средней концентрации. Этот вывод подтверждается также экспериментами по изучению релаксации в веществах, облученных при 300 К протонами с энергией 4 35 Мэв. В случае a - аланина оказалось, что величины ( Тв) 1 и а на начальном участке накопления для образцов, облученных протонами, практически совпадают с этими величинами для - - облученных образцов. Это означает, что характер распределения радикалов в данном случае не зависит от характера распределения ионов при радиолизе. [12]
При 20 арильный радикал реагирует со вторым радикалом примерно с 103 - 104 раз большим выходом столкновений, чем с молекулой толуола в растворителе. Таким образом, в том случае, когда образование бензил-толуола становится важным, концентрация бензильного радикала должна быть порядка 10 - 2 моль. Для создания этой высокой концентрации радикалов необходима очень высокая локальная интенсивность дозы. Это означает, что только некоторые из шпор содержат бензильный радикал и что реже встречаются шпоры больше чем с одним радикалом. Можно оценить средний объем шпор, в которых отдельные радикалы создают среднюю концентрацию радикалов, равную 1СГ2 моль. [13]
Страницы: 1