Постоянная концентрация - компонент
Cтраница 2
Это равенство показывает, что ос постоянна только при постоянной концентрации компонентов. В этой связи представляется целесообразным найти дифференциальное уравнение размывания для скорости потока. [16]
С - переменная по толщине слоя концентрация; Сж - постоянная концентрация компонента в потоке. [17]
Анализ, выполненный в [49, 50], показывает, что заряд электрода Q, входящий в термодинамические соотношения, равен тому количеству электричества, которое необходимо сообщить электроду при увеличении его поверхности на единицу и сохранении постоянной концентрации компонентов раствора. Под гиббсовскими адсорбциями Г компонентов следует понимать те количества соответствующих веществ, которые необходимо ввести в систему для поддержания постоянства объемных фаз при увеличении поверхности раздела на единицу. [18]
При постоянных концентрациях компонентов на входе реактора концентрация бромид-иона, одного из реагирующих компонентов, обнаруживает сложное субгармоническое поведение, зависящее от скорости потока через реактор. [19]
В отличие от электролитического никелирования химический процесс сопровождается быстрым истощением раствора и резким падением скорости осаждения. При электролитическом отложении постоянная концентрация компонентов ванны поддерживается за счет непрерывного растворения анодов. В ряде растворов скорость осаждения практически прекращается после 2 - 3 ч работы ванны. При корректировании состава электролита ванну останавливают каждый час для добавления компонентов. [20]
В связи с тем что процесс осаждения хрома происходит с использованием нерастворимых анодов, состав электролитов при электролизе непрерывно изменяется. Поэтому для поддержания постоянной концентрации компонентов электролиты периодически корректируют в соответствии с результатами химических анализов и через каждые 2 - 3 ч работы добавляют из ванны улавливания недостающий объем воды. [21]
Были также изучены серии растворов при постоянных концентрациях компонентов, но переменном значении рН растворов. На основании последней серии опытов были построены кривые D / ( рН), детальный анализ которых позволил авторам установить состав комплексов и рассчитать константы равновесия и константы диссоциации образуемых комплексов. [22]
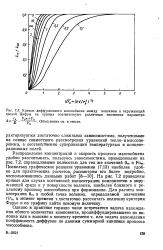 |
Кривые диффузионного массообмена между волокном и окружающей средой. Цифры на кривых соответствуют различным значениям параметра. [23] |
Распределение концентраций и скорость процесса маюсообмена удобно рассчитывать, пользуясь зависимостями, приведенными на рис. 7.2, справедливыми полностью для тех же значений 9т и Fom. На рис. 7.2 приведены кривые для случая постоянной концентрации компонентов в окружающей среде и у поверхности волокна, наиболее близкого к реальному процессу массообмена при формовании. Для расчета концентрации 6т в любой точке волокна, определяемой значением г / г3, в момент времени т достаточно рассчитать величину критерия Фурье и по графику найти искомую величину. [24]
Первый способ заключается в том, что в колонку вводят газовую смесь с постоянной концентрацией компонентов. [25]
Следует отметить, что при подборе второго растворителя, кроме эффекта повышения растворяющей способности и избирательности первого растворителя, следует учитывать возможность его выделения из растворов с углеводородами. Одним из моментов, осложняющих применение смешанных растворителей, является трудность их регенерации и поддержание в процессе эксплуатации постоянной концентрации компонентов в составе растворителя. Поэтому при выборе второго растворителя желательно, чтобы добавляемый растворитель, кроме удовлетворения требованиям, предъявляемым к обычным избирательным растворителям, хорошо смешивался с первым, и его температура кипения была равной или близкой температуре кипения основного растворителя, или же температура кипения добавляемого растворителя должна быть значительно более низкой, чем углеводородного сырья. Только при удовлетворении всем этим требованиям вторичный растворитель может быть успешно использован. [26]
Поскольку активность и химический потенциал компонента при постоянной температуре связаны между собою взаимнооднозначной зависимостью ( 44), причем возрастание химического потенциала всегда соответствует возрастанию активности, то при качественном обсуждении состояния систем и их зависимости от внешних условий оба понятия для нас равносильны. Но понятие молярной доли или концентрации компонента в ряде случаев даже при качественном рассмотрении систем приходится противополагать понятию активности или химического потенциала, так как нередко при постоянной концентрации компонента его активность или химический потенциал могут изменяться или наоборот, в особенности в результате химического взаимодействия компонентов в растворе. Мы уже отмечали, что при ин-фильтрационном метасоматозе в число факторов равновесия входят концентрации вполне подвижных компонентов в поровых растворах, вместо их химических потенциалов или активностей при диффузионном метасоматозе. [27]
 |
Принципиальная схема установки УПО-1. [28] |
Дополнительная погрешность, вызванная изменением температуры окружающей среды на 5 С ( от 20 С), не превышает 5 % от измеряемой величины. Время, в течение которого установленное значение концентрации компонентов в смеси остается постоянным, составляет не менее 120 мин. Время установления постоянной концентрации компонентов в смеси от момента подачи смеси внутри одного диапазона не превышает 10 мин, а при переходе с одного диапазона на другой - 20 мин. [29]
Начальный участок связан с формированием концентрационного профиля в жидкой фазе. Характеристическое расстояние, соответствующее установлению постоянной концентрации компонента в твердой фазе CSC0, приблизительно равно D / ( / Cof) и, следовательно, может составлять от нескольких микрометров до нескольких сантиметров. Конечный нестационарный участок обусловлен приближением межфазовой границы к концу образца и повышением средней концентрации примесного компонента в жидкой фазе. [30]
Страницы: 1 2 3