Низкая концентрация - сероводород
Cтраница 1
Низкие концентрации сероводорода при переработке угля СРК облегчают выбор потенциальных катализаторов, в качестве которых интерес могут представить многие сложные оксиды, бориды, карбиды и нитриды. Новые методы синтеза открывают возможность приготовления некоторых из этих веществ в виде образцов с высокоразвитой поверхностью, что необходимо для их применения в катализе. [1]
При низких концентрациях сероводорода ( - 2 мг / л) продукты коррозии состоят из троилита и пирита. В диапазоне концентраций от 2 до 20 мг / л в них дополнительно содержится канзит. [2]
При низких концентрациях сероводорода протягивают 250 мл исследуемого воздуха в течение 3 мин. В случае если индикаторный порошок окрасится полностью, определение повторяют, о протягивают только 30 мл воздуха в течение 2 мин. [3]
Однако при низкой концентрации сероводорода ( 10 мг / л) защита слабая. [4]
Сложные карбиды нестабильны при высоких концентрациях сероводорода, но некоторые композиции, по-видимому, стабильны при низких концентрациях сероводорода. Они сохраняют металлические характеристики с повышенной термической стабильностью. Возможная область применения - метанирование Простые нитриды являются промежуточными соединениями, имеют высокую термическую стабильность, огнеупорность и твердость. Они нестабильны при высоких концентрациях сероводорода, при низких концентрациях сероводорода более стабильны, чем карбиды. Изучены в синтезе Фишера - Тропша Сложные нитриды менее огнеупорные, чем простые. [5]
В качестве нейтрализатора сероводорода в буровом растворе на месторождениях, содержащих высокие концентрации сероводорода в нефтяном газе, рекомендуется применять флотационный концентрат, ai на месторождениях, содержащих низкие концентрации сероводорода ( до 1 %) - шламовый отход. [6]
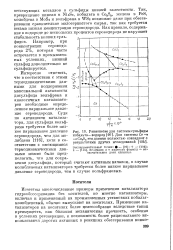 |
Равновесие для системы сульфиды кобальта-водород [ 901. Для системы Со - - Со 88 эти данные полностью совпадают с результатами других исследований [ 1041. [7] |
Так, превращение никеля в NisSa, кобальта в Co9S8, железа в FeS, молибдена в МоЗг и вольфрама в WS2 возможно даже при обессе-ривангш сравнительно малосернистого сырья, так как требуется весьма низкая концентрация сероводорода. Как правило, содержание в водороде до нескольких процентов сероводорода не нарушает стабильность низших сульфидов. Например, при концентрации сероводорода 2 %, которая часто встречается в промышленных условиях, низший сульфид дополнительно не сульфидируется. [8]
При низких концентрациях сероводорода образуются пленки, еоеюмщие в основном из пирита FeS2 и троилита FeS. При увеличении концентрации сероводорода, в пленке увеличивается содержание канзита Fe S s, который не обладает защитными свойствами. [9]
Одним из перспективных направлений переработки таких газов является процесс каталитического окислительного превращения сероводорода в элементарную серу в газовой фазе на твердых катализаторах. При низких концентрациях сероводорода окисление его удается осуществлять в стационарном слое катализатора при температуре до 300 С. При концентрации сероводорода выше б % об. возникают трудности проведения процесса окисления в стационарном слое ката-лизатора из-за значительной экэотермичности - реакции. Азизбекова предлагается проводить окисление высококонцентрированного сероводорода в несколько стадий с раздельной подачей кислорода на каждую каталитическую ступень. Например, для окисления сероводорода концентрацией 25 % об, потребуется пять реакторов, т.е. предлагается такой технологический режим, при котором в одном реакторе окисляется 4 - 5 % сероводорода. [10]
Одним из перспективных направлений переработки таких газов является процесс каталитическогоокислительного превращения сероводорода в элементарную серу газовой фазе на твердых катализаторах. При низких концентрациях сероводорода окисление его удается осуществлять в стационарном слое катализатора при температуре до 300 С. При концентрации сероводорода выше б % об. возникают трудности проведения процесса окисления в стационарном слое катализатора из-за значительной экэотврмичнооти реакции; Поэтому со-грудниками АэИНШТЕХИМ им. Аэизбекова предлагается проводить окисление высококонцентрированного сероводорода в несколько стадий с раздельной подачей кислорода на каждую каталитическую ступень. Например, для окисления сероводорода концентрацией 25 % об. потребуется пять реакторов, т.е. предлагается такой технологический режим, при котором в одном реакторе окисляется 4 - 6 % сероводорода. [11]
 |
Минимальная концентрация сероводорода. [12] |
Примеры, приведенные в табл. 9 - 3, показывают, что тенденция к сульфидированию переходных металлов сохраняется в широких пределах. Однако при низких концентрациях сероводорода картина меняется. Например, в условиях метанирования ( содержание сероводорода менее 1 млн -) сульфидные катализаторы ( NiS) нестабильны, но все - же существует значительное взаимодействие сероводорода с поверхностью катализатора. [13]
Сардиско и Греко [192] провели всестороннее исследование состава продуктов коррозии, возникающих в средах, содержащих сероводород. Рентгеноструктурным анализом показано, что сульфиды, образующиеся при низких концентрациях сероводорода ( до 2 0 мг / л), состоят из троилита Fe7S8 и пирита FeS с размерами кристаллов до 200 А. При концентрациях H2S от 2 0 до 20 мг / л дополнительно появляется небольшое количество кансита FegSs. При концентрациях H2S от 20 до 600 мг / л в продуктах коррозии преобладает кансит и уменьшается содержание троилита. Размеры кристаллов при этом увеличиваются до 750 А. Сульфиды, образующиеся на поверхности металла при pH 6 5 - f - 8 8, состоят в основном из кансита и обладают наименьшими защитными свойствами. Сульфиды, возникающие при других значениях рН, состоят из троилита и пирита и отличаются более высокими защитными свойствами. Герцог [193] считает, что сернистое железо общей формулы FexSy нестехиометрического состава обладает полупроводниковыми свойствами. Во многих работах было показано, что разница в потенциалах железа и сульфида железа может составить 0 2 - 0 4 В. [14]
Использование раствора МЭА, хорошо поглощающего как H2S, так СОз, не позволяет селективно выделить сероводород, и при его выделении после регенерации получаются газы, в которых соотношение H2S и СО2 остается таким, каким оно было в очищаемом газе. В случае очистки раствором МЭА газа газификации нефтяных остатков в кислых газах получается низкая концентрация сероводорода. Такой газ нецелесообразно использовать в производстве серы, поэтому применение раствора МЭА для очистки в этом случае не рекомендуется. [15]
Страницы: 1 2