Более низкая концентрация
Cтраница 2
При более низкой концентрации получается слишком слабая денитрованная кислота, повышение же концентрации выше 70 % снижает мощность денитрационной колонны. [16]
При более низкой концентрации SO2 не обеспечивается автотермичность процесса, при более высокой-понижается степень контактирования. [17]
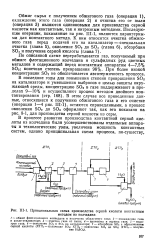 |
Принципиальная схема производства серной кислоты контактным. [18] |
При более низкой концентрации SO2 не обеспечивается автотермичность процесса. [19]
При более низкой концентрации SO2 не обеспечив § § тод аутотермичн61лч7 юцесса, принесшее высоком понижается степень контактирования. [20]
При более низкой концентрации невозможно нормально осуществлять пуск и обеспечивать стабильную работу центрифуги из-за нарушения процесса фильтрации в зоне хода толкателя, в результате чего жидкость, которая не успела отфуговаться, попадает в зону сушки и частично вымывает осадок. Вымывание начинается обычно у уравнительного кольца и распространяется к месту выгрузки осадка. При этом работа центрифуги сопровождается сильной вибрацией. Снижение концентрации суспензии до 20 % и ниже приводит к попаданию жидкости в бункер осушенного продукта. [21]
 |
Принципиальная схема производства серной кислоты контактным. [22] |
При более низкой концентрации SO2 не обеспечивается автотермичность процесса. [23]
 |
Принципиальная схема производства серной кислоты контактным. [24] |
При более низкой концентрации 5СЬ не обеспечивается автотермичность процесса. [25]
При более низкой концентрации снижается скорость образования золя и уменьшается однородность частиц. [26]
 |
Схема очистного отделения контактной системы фирмы Лурги. [27] |
При более низкой концентрации SO2 не обеспечивается аутотермичность процесса, при более высоком содержании понижается степень контактирования. [28]
При более низкой концентрации имеется свободный растворитель и эту систему можно рассматривать как растворы соли в воде. Выше этого предела свободного растворителя нет; при возрастании концентрации электролита происходит только перераспределение воды в сольватных сферах в пользу более гидрофильного иона и система является как бы раствором воды в раздвинутой решетке электролита. Реальность этой границы была под-тиерждена рядом независимых методов. [29]
При более низкой концентрации имеется свободный растворитель и эту систему можно рассматривать как растворы соли в воде. Выше этого предела свободного растворителя нет; при возрастании концентрации электролита происходит только перераспределение воды в сольватных сферах в пользу более гидрофильного иона и система является как бы раствором воды в раздвинутой решетке электролита. Реальность этой границы была подтверждена рядом независимых методов. [30]
Страницы: 1 2 3 4 5