Поверхностная концентрация - адсорбированная молекула
Cтраница 1
Поверхностная концентрация адсорбированных молекул ZnEt2, по данным Фурукавы 203, оценивается величиной порядка 3 - Ю14 - 4 - 10й молекул / см2, что близко к монослойному заполнению. Адсорбция не является, видимо, достаточно прочной, поскольку двукратная промывка катализатора чистым растворителем приводит к резкому падению его активности. [1]
Поверхностная концентрация адсорбированных молекул ZnEt2, по данным Фурукавы 203, оценивается величиной порядка 3 - Ю1 - 4 - 1014 молекул. Адсорбция не является, видимо, достаточно прочной, поскольку двукратная промывка катализатора чистым растворителем приводит к резкому падению его активности. [2]
Снижение полярографических максимумов в присутствии органических веществ объясняется изменением поверхностной концентрации адсорбированных молекул при движении ртутной поверхности. Например, при движении ртути от нижней части к шейке капли происходит растяжение поверхности нижней части капли, поверхностная концентрация адсорбированного вещества на этом участке понижается, а пограничное натяжение соответственно повышается. Наоборот, в верхней части капли происходит увеличение поверхностной концентрации органического вещества, снижающее пограничное натяжение. Поэтому возникает сила, действующая в направлении от шейки к нижней части капли и вызывающая ослабление, а в определенных условиях и полное прекращение тангенциальных движений поверхности. Кроме того, необходимо учитывать, что в области адсорбции органического вещества электрокапиллярная кривая становится, как правило, более плоской и различия в пограничном натяжении между разными участками капли уменьшаются. [3]
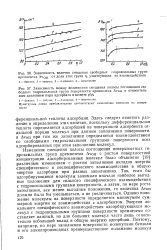
Изменение смещения полосы поглощения поверхностных гидроксильных групп кремнезема AVOH с ростом поверхностной концентрации адсорбированных молекул было объяснено [19] различным изменением с ростом заполнения вкладов энергии специфического и неспецифического взаимодействия в общую энергию адсорбции при разных заполнениях. Так, если бы адсорбирующиеся молекулы занимали вначале наиболее выгодные положения для сильного специфического взаимодействия с гидроксильными группами поверхности, а затем, по мере роста заполнения, все менее выгодные положения, то величина AVOH должна была бы уменьшаться, а не увеличиваться. Однако положение молекулы на поверхности определяется минимумом суммарной энергии ее взаимодействия с адсорбентом. Энергия локального специфического взаимодействия адсорбирующихся молекул с гидроксильными группами поверхности кремнезема составляет важный, но для больших молекул часто лишь относительно небольшой вклад в общую энергию адсорбции. [5]
Все изложенное находится в удивительном соответствии с работой [1], где указывается, что понижение поверхностной концентрации адсорбированных молекул заметно повышает скорость падения поляризации, что согласуется с предположением о внедрении пленки поверхностно-активных веществ между обкладками двойного слоя. Гц, а при 5 Гц осадок темный, грубокристаллический. Столько же времени нужно, чтобы потенциал после спада самопроизвольно возрос до значений, отвечающих наличию плотной адсорбционной пленки ПАВ на поверхности электрода ( рис. 2, 1), Интересно в этой связи, что Дж. [7]
Различие в толщине пленок для растворов одних и тех же ПАВ в октане и ксилоле следует объяснить неодинаковой поверхностной концентрацией адсорбированных молекул. В адсорбционные слои входят молекулы растворителя и, следовательно, молекулы ПАВ расположены под углом к границе раздела фаз. Проникновение бензола в адсорбционные слои моноглицерида пальмитиновой кислоты доказано спектроскопическим методом Ределем. [8]
Поскольку величина ks определяется из столкновений с поверхностными атомами, так же как и с другими адсорбированными атомами, то она относительно мала и на нее значительно менее влияет поверхностная концентрация адсорбированных молекул. [9]
Во всех случаях торможение разряда, сопровождающегося появлением низкого предельного тока, продолжается до достижения потенциала начала заметной десорбции добавок с поверхности электрода, после чего по мере уменьшения поверхностной концентрации адсорбированных молекул наблюдается значительное увеличение тока с поляризацией. Повышение температуры и уменьшение концентрации добавок резко увеличивают предельный ток и понижают поляризацию процесса. [10]
В общем случае реагирующий пик, двигаясь, изменяет не только свою площадь, но и свою форму. В сечении х при р f рх на поверхности этому соответствует равновесная или неравновесная поверхностная концентрация адсорбированных молекул. [11]
В общем случае реагирующий пик, двигаясь, изменяет но только свою площадь, но и свою форму. В сечеппн х при р 1 рх на поверхности этому соответствует равновесная или неравновесная поверхностная концентрация адсорбированных молекул. [12]
Страницы: 1