Эквивалентная концентрация
Cтраница 3
Раствор с эквивалентной концентрацией 1 г-экв растворенного вещества на 1 л раствора называется нормальным ( н) раствором. [31]
С - - эквивалентная концентрация / - и соли, моль / л; аг-е - эквивалентная электропроводность раствора / - и соли ( См / см), соответствующая суммарной эквивалентной концентрации С. [32]
 |
Распределение эквивалентной концентрации катионов ( Ск, анионов ( Са и электролита в целом ( С вблизи поверхности электрода mm. [33] |
На участке 8 эквивалентные концентрации катионов и анионов уже одинаковы и точка а отмечает конец двойного слоя. Концентрация в точке Ь равна общей концентрации в глубине раствора, не измененной за счет процесса, текущего на электроде. Расстояние 8, на котором концентрация претерпевает изменение, называется толщиной диффузионного слоя. [34]
От массовой или эквивалентной концентрации с удельная проводимость зависит нелинейно. [35]
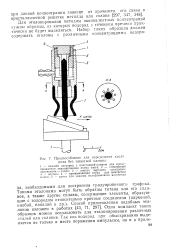 |
Приспособление для определения кислорода без защитной камеры. [36] |
Для эталонирования методом эквивалентных концентраций нужны образцы, из которых водород с течением времени практически не будет выделяться. [37]
При смешивании растворов различных эквивалентных концентраций получается раствор, концентрация которого определяется общим числом эквивалентов в 1 л раствора. [38]
При смешивании растворов различных эквивалентных концентраций получается раствор, концентрация которого определяется общим числом эквивалентов в I л раствора. [39]
Все анионы при эквивалентной концентрации дают одинаковые предельные токи, только предельный ток ионов, гидроксила приблизительно вдвое превышает предельный ток других анионов. [41]
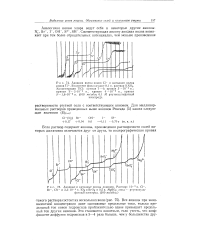 |
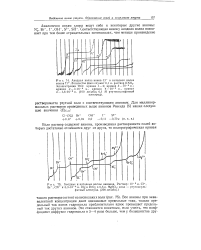
Анодные и катодные волны анионов. Раствор. 10 3 н. С1 -, Br -, CN и 3 3 - 10 - 4 н. Юз и ВгОд в 0 5 н. MgSO4. анод - ртутносульфатный электрод. ( 200 мв / абсц. [42] |
Все анионы при эквивалентной концентрации дают одинаковые предельные токи, только предельный ток ионов гидроксила приблизительно вдвое превышает предельный ток других анионов. [43]
Серная кислота при эквивалентной концентрации водородных ионов обладает примерно такой же коррозионной активностью, как и соляная кислота. Скорость коррозии железа возрастает с увеличением концентрации H2S04, достигая максимума в 47 % - ной H2SO4, после чего уменьшается, а при 100 % - ной концентрации резко повышается. [44]
Серная кислота при эквивалентной концентрации водородных ионов обладает примерно такой же коррозионной активностью, как и соляная кислота. Скорость коррозии железа возрастает с увеличением концентрации H2SO4, достигая максимума в 47 % - ной H2SO4, после чего уменьшается, а при 100 % - ной концентрации резко повышается. [45]
Страницы: 1 2 3 4