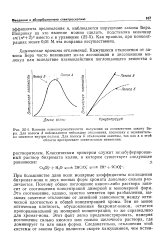
Общая концентрация - хром
Cтраница 1
Общие концентрации хрома и тиоцианата в различных фракциях получались следующим образом: добавляли щелочь для разложения комплекса и осаждения большей части хрома в виде гидроокиси, которую затем отфильтровывали, превращали в бихромат, и хром определяли иодометрически. [1]
При постоянном рН с ростом общей концентрации хрома это равновесие сдвигается вправо и доля ионов СгО уменьшается, а доля Сг20 - растет. [2]
Она имеет первый порядок по общей концентрации хрома и почти не зависит от концентрации перекиси до тех пор, пока последней не останется очень мало. [3]
При этих разбавлениях фактическая концентрация бихромата в растворе будет изменяться приблизительно пропорционально квадрату общей концентрации хрома. [4]
При работе электролита в него периодически добавляют хромовый ангидрид. В результате добавления СгО3 общая концентрация хрома в растворе постепенно возрастает. [5]
Вместо бихромат-ионов в растворе появляются гидрохромат и хромат-ионы. Так как есгго-7 и есю -, различны, зависимость оптической плотности от общей концентрации хрома в растворе не будет линейной. [6]
На основании предварительных исследований были выделены четыре фактора, оказывающие основное влияние на выход по току У ( в %): общая концентрация хрома в растворе Ссг, концентрация хлора в растворе ( в расчете на НС1) Сн. Две последние величины отнесены к единице поверхности пары мембран, содержащихся в ячейке. [7]
При работе ванны в нее периодически добавляют хромовый ангидрид. Расход его на 1 м2 оксидируемой поверхности составляет в среднем: для 3-процентного раствора хромового ангидрида 10 г, для 9 5-процентного раствора 30 г. В результате добавления СгОз общая концентрация хрома в растворе возрастает. По достижении указанной концентрации электролит должен быть разбавлен водой или заменен новым. [8]
При большинстве длин волн молярные коэффициенты поглощения бихромат-иона и двух ионных форм хромата довольно сильно различаются. Поэтому общее поглощение какого-либо раствора зависит от соотношения концентраций димерной и мономерной форм. Это соотношение, однако, заметно меняется при разбавлении, вызывая заметное отклонение от линейной зависимости между оптической плотностью и общей концентрацией хрома. Тем не менее оптическая плотность, обусловленная бихромат-ионом, остается пропорциональной их молярной концентрации; то же справедливо для хромат-иона. Этот факт легко продемонстрировать, измеряя поглощение сильно кислого или сильно щелочного раствора, где доминирует та или иная форма. [10]
Электролиз в растворах хромовой кислоты осуществляется с нерастворимыми анодами. Применение растворимых хромовых анодов невозможно ввиду того, что анодный выход хрома по току в 6 - 8 раз выше катодного. Кроме того, при анодном растворении хрома в раствор наряду с шестивалентным хромом переходит трехвалентный. Благодаря этому в электролите непрерывно возрастает общая концентрация хрома и накапливаются значительные количества трехвалентных его соединений, что нарушает нормальное течение электролиза. [11]
Страницы: 1