Стационарная концентрация - продукт - реакция
Cтраница 1
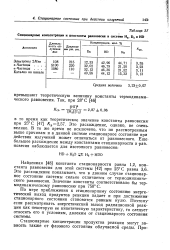 |
Стационарные концентрации и константы равновесия в системе Н, D, и HD. [1] |
Стационарные концентрации продуктов реакции могут зависеть также от фазового состояния облучаемой среды. [2]
Абсолютные величины стационарных концентраций продуктов реакции часто значительно превышают термодинамические равновесные концентрации для идентичных условий. Так, стационарная концентрация озона при облучении жидкого кислорода равна 0 8 мол. С практически равна нулю. Стационарная концентрация NO2 при облучении газообразной смеси азота с кислородом при 20 С быстрыми электронами с интенсивностью порядка 1015 эв сек-1 см-3 составляет около 6 объемн. По условиям термодинамического равновесия в этом случае концентрация NO2 также практически равна нулю. [3]
Абсолютные величины стационарных концентраций продуктов реакции часто значительно превышают термодинамические равновесные концентрации для идентичных условий. Так, стационарная концентрация озона рри облучении жидкого кислорода равна 0 8 мол. С практически равна нулю. Стационарная концентрация NO2 при облучении газообразной смеси азота с кислородом при 20 С быстрыми электронами с интенсивностью порядка 1015 эв сек-1 см-3 составляет около 6 объемн. По условиям термодинамического равновесия в этом случае концентрация NO2 также практически равна нулю. [4]
Для реакций простых типов характерно уменьшение стационарной концентрации продукта реакции и увеличение стационарной концентрации исходного вещества по мере увеличения скорости массообмена. [6]
Помимо этого способа, величина ф может быть определена по распределению стационарных концентраций продукта реакции нулевого порядка по длине реактора. [7]
IV показано, что в реакции первого порядка стационарная концентрация исходного вещества растет, а стационарная концентрация продукта реакции падает с увеличением и. Нетрудно убедиться, что это имеет место и в более сложном случае двух последовательных реакций первого порядка. [8]
IV было показано, что в случае реакции первого порядка стационарная концентрация исходного вещества растет, а стационарная концентрация продукта реакции падает с увеличением и. Нетрудно убедиться, что это имеет место и в более сложном случае двух последовательных реакций первого порядка. [9]
Это положение, по-видимому, является истинным только для относительно простых систем. Так, в реакции инги-бированного a - нафтолом окисления я-декана в открытой системе было установлено, что стационарные концентрации продукта реакции ( гидроперекиси) и ингибитора зависят от начальной концентрации ингибитора в системе. [10]
Известно, что многие реакции, протекающие в проточной системе, следует рассматривать как самотормозящиеся процессы со стационарной концентрацией продуктов реакции. Значительное отравляющее действие воды и водорода, по-видимому, согласуется с представлениями Шваба [1], считающего, что при реакции происходит переход электронов от муравьиной кислоты к никелю и что этот процесс тормозится накоплением электронов за счет адсорбции воды и водорода. [11]
Увеличение интенсивности материального обмена приводит к повышению стационарной концентрации исходных веществ. В случае реакторов полного смешения, когда параметры aj ( характеризующие интенсивность материального обмена со средой различных компонентов реакции, для всех компонент реакции одинаковы, повышение интенсивности обмена приводит к уменьшению стационарной концентрации продуктов реакции. [13]
Если например, фермент катализирует реакцию, в ходе которой изменяется рН среды, то рН - чувствительный электрод, гюкры-тый пленкой геля или полимера, содержащей этот фермент, позволит провести количественное определение только того вещества, которое превращается под действием данного фермента. Если ионселективный электрод, чувствительный к ионам NH, покрыть пленкой, содержащей уреазу, то при помощи его можно количественно определять мочевину. Концентрацию исследуемого вещества ферментными электродами можно определить тремя способами: регистрируя показания электрода при проведении ферментативной реакции до конца ( до полного превращения субстрата); измеряя скорость изменения показаний электрода в начальный период реакции; регистрируя показания электрода в момент установления стационарного потенциала, который соответствует стационарной концентрации продукта реакции в приэлектродном слое. На практике обычно применяют два последних способа. Уже разработано более 50 различных ферментных электродов, причем имеются электроды для определения не только субстратов, но и самих ферментов. В некоторых ферментных электродах используют вместо очищенных ферментов живые бактериальные и микробные клетки. Разрабатываются иммуноэлектроды и гормоночувствительные мембранные электроды. [14]
В начале опыта потенциал электрода ( измерявшийся в вольтах) был равен нулю. Независимо от времени предварительной анодной обработки и плотности тока на процесс катодного восстановления ( a b на рис. 82) всегда затрачивалось около 4 - 10 - 4 кулон см-2, причем это не зависело также от плотности катодного тока. На основании этого Тернер заключил, что в данном электролите анодное окисление сопровождается всегда образованием на поверхности электрода одной и той же стационарной концентрации продуктов реакции. При истолковании этих результатов Тернер полагал, что на аноде создается монослой двуокиси германия или гидроокиси германия и что для полного протекания процесса восстановления на каждый участок поверхности германия требуется четыре электрона. [15]
Страницы: 1 2

