Критическая концентрация - антиоксидант
Cтраница 2
Внесение в полимер сульфида R2S в достаточной концентрации, даже если б 1, может сделать знаменатель в правой части уравнения ( 26) положительным, что позволит реализоваться критической концентрации антиоксиданта. [17]
В Советском Союзе в основу теоретических работ по стабилизации и деструкции полимеров были положены представления академика Н. Н. Семенова о цепных реакциях с вырожденными разветвлениями. Советские ученые разработали теорию критических концентраций антиоксидантов и показали, что процессы стабилизации имеют очень сложный химический характер; существенную роль в них играют сами полимеры. Следовательно, для полимеров различной структуры требуются и различные стабилизаторы. Кроме того, было показано, что применявшиеся до сих пор антиоксиданты, наряду с обрывом цепей, могут также инициировать окисление и вызывать вырожденные разветвления. [18]
Однако если принять, что механизм действия антиоксидантов сводится только к реакции антиоксиданта с RO2, то образующаяся при этом гидроперекись, распадаясь по реакции ( IV) на радикалы RO и R, может дать начало новым цепям. Если при распаде перекиси образуется больше одного или один активный центр, начинающий новую цепь, то критическая концентрация антиоксиданта не может иметь места. [19]
Однако если принять, что механизм действия антиоксидантов сводится только к реакции антиоксиданта с RO2 то образующаяся при этом гидроперекись, распадаясь по реакции ( IV) на радикалы RO и R, может дать начало новым цепям. Если при распаде перекиси образуется больше одного или один активный центр, начинающий новую цепь, то критическая концентрация антиоксиданта не может иметь места. [20]
Кривые расходования этого антиоксиданта трансформировались в прямые линии в координатах реакции первого порядка, однако эти линии не всегда проходили через начало координат, что было объяснено существованием верхней критической концентрации антиоксиданта. Избыток антиоксиданта сверх верхней критической концентрации расходовался с большой скоростью в первые минуты окисления, после чего процесс резко замедлялся и остаток фенил-р-нафтиламина расходовался с относительно низкой скоростью по закону первого порядка до достижения нижней критической концентрации, когда процесс вновь ускорялся. [21]
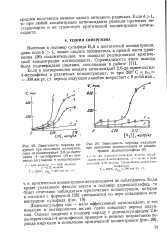
При значениях х - - со свободный член равен - со, при х О свободный член отрицателен, что отвечает нестационарной реакции. Кривые на рис. 18 изображают два варианта парабол, отвечающих указанным выше условиям. Кривая 1 не пересекает ось абсцисс, что соответствует нестационарной реакции при любых концентрациях антиоксиданта. Значение xt отвечает хорошо известной критической концентрации антиоксиданта. Это значит, что должен существовать верхний предел х2 концентрации антиоксиданта, выше которого мы снова попадаем в область нестационарной реакции окисления. Таким образом, при х х и при х жа должна наблюдаться автоускоряющаяся реакция, причем скорость расхода антиоксиданта должна быть велика. [22]
При значениях х со свободный член равен - оо, при х О свободный член отрицателен, что отвечает нестационарной реакции. Кривые на рис. 18 изображают два варианта парабол, отвечающих указанным выше условиям. Кривая 1 не пересекает ось абсцисс, что соответствует нестационарной реакции при любых концентрациях антиоксиданта. Значение х отвечает хорошо известной критической концентрации антиоксиданта. Стационарная реакция протекает только при значениях х, лежащих между хг и а. Это значит, что должен существовать верхний предел х2 концентрации антиоксиданта, выше которого мы снова попадаем в область нестационарной реакции окисления. Таким образом, при х х1 и при х хг должна наблюдаться автоускоряющаяся реакция, причем скорость расхода антиоксиданта должна быть велика. [23]
Страницы: 1 2