Высокая концентрация - кислота
Cтраница 1
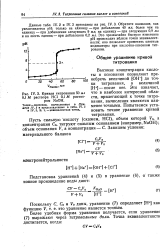 |
Кривая титрования 50 мл 0 1 М раствора НС1 0 1 М раствором NaOH. [1] |
Высокие концентрации кислоты и основания позволяют пренебречь величиной [ ОН - ] до точки титрования, а величиной [ Н ] - после нее. Это означает, что в наиболее интересной области, прилегающей к точке титрования, вычисления являются наименее точными. [2]
Высокая концентрация кислоты обычно затрудняет фильтрование. Если оставить реакционную смесь стоять в течение 1 часа в бане со льдом, то твердое вещество плотно соединится в единую массу, после чего жидкость можно легко фильтровать с небольшим отсасыванием или же декантировать. [3]
Высокую концентрацию кислоты невыгодно держать еще и потому, что при этом увеличивается количество моногидрата, передаваемого из абсорбционного отделения для закрепления сушильной кислоты, и, следовательно, увеличивается количество кислоты, возвращаемое в абсорбционное отделение. [4]
При высокой концентрации кислот в продуктах окисления циклогексана определение циклогексанона по вышеприведенной методике дает заниженные результаты. Это связано с тем, что соли, образовавшиеся после предварительной нейтрализации кислот, реагируют с НС1, выделяющейся при реакции кетона с гидроксиламином, и вновь образуют карбоновые кислоты. При рН перехода индикатора эти кислоты оттитровывают ся Не полностью. [5]
При высоких концентрациях кислоты и кобальта даже ов тех случаях, когда осаждение проводится при очень высоких плотностях тока, нельзя достигнуть достаточно высокого выхода по току. [6]
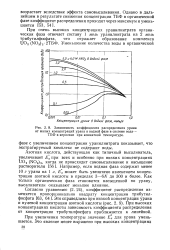 |
Зависимость коэффициента распределения урана. [7] |
При высоких концентрациях кислоты зависимость коэффициента распределения от концентрации трибутилфосфата приближается к линейной. [8]
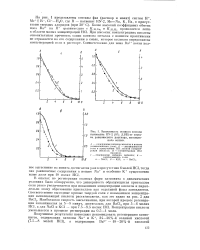 |
Зависимость ионного состава л п катионита КУ-2 ( 8 % ДВЕ от соста-ва равновесного раствора, насыщенного солыо. [9] |
IIppi высоких концентрациях кислоты относительная прочность связи катиона металла с ионитом практически не отражается на его содержании в смоле, которое целиком определяется концентрацией соли в растворе. [10]
При высоких концентрациях кислоты, когда образуется желтый пермолибдат ( не установлено, имеет ли он формулу HMoOfT или Н2МоО6), а также при больших концентрациях щелочи, когда нет никаких видимых признаков образования какого-либо пермолибдата, скорость разложения исключительно мала. В нейтральном растворе, однако, наблюдаются две странные особенности. Во-первых, та же скорость с данным катализатором возможна только в том случае, если катализатор предварительно обработан перекисью водорода и применяется тотчас же после этого. Во-вторых, скорость реакции с таким предварительно обработанным катализатором обнаруживает при концентрации перекиси около 0 01 М максимум, которого нет в кислых или щелочных растворах. Это напоминает поведение хромата в слабокислых растворах. [11]
При высоких концентрациях кислоты практически весь метанол может быть превращен в инертный ион метилоксония и скорость этерификации может стать очень малой, несмотря на присутствие оксониевого иона уксусной кислоты. [12]
При высоких концентрациях кислоты возможна адсорбция на ионитах нейтральных комплексных форм, поляризующихся под действием высокополярных ионогенных групп ионита. Исключительно большая способность полония к сорбции на анионитах используется для отделения Ро от ряда элементов, образующих более слабые ацидокомплексы. [13]
Большой частью высокая концентрация кислоты наблюдается в золе и шлаке, отлагающихся на трубах. [14]
Несмотря на высокую концентрацию кислот в отдельных фракциях газойля доля кислот высокой молекулярной массы в их общем содержании в нефтях является весьма значительной, особенно в тяжелых нефтях. [15]
Страницы: 1 2 3 4