Высокая концентрация - окислитель
Cтраница 1
 |
Схема химического контроля водного режима блока 300 МВт. [1] |
Высокие концентрации окислителя небезопасны для конвективных поверхностей нагрева, выполненных из эустенитной стали, с точки зрения коррозионного разрушения. [2]
Однако добавление этого количества озона к атмосферному воздуху с высокой концентрацией окислителей усиливает поражение, характерное для смога, а не для озона. Вероятно, содержание озона в воздухе, в дни, когда уровень окислителей к ним низок, не совсем достаточно для проявления его токсического действия, тогда как при высоких концентрациях окислителей озон реагирует преимущественно с другими компонентами атмосферы, образуя избыток токсических веществ смога. [3]
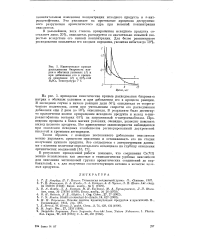 |
Кинетические кривые расходования бихромата натрия в обычных условиях ( 1 и при добавлении его в процессе окисления ( 2 в 60 % - ной H2S04. Температура 7 С. [4] |
Это указывает на протекание процессов деструктивного разрушения ароматического ядра при высокой концентрации окислителя. [5]
Получаемые по этому способу фосфатно-оксидные покрытия по внешнему виду мало отличаются от пленок, образуемых при щелочном оксидировании ( воронении), а по принципу своего образования и составу электролита относятся к типу пленок, получаемых при фосфатировании. Вследствие высокой концентрации окислителя возрастает скорость возникновения зародышей кристаллов и количество их, в результате чего рост отдельных кристаллов ограничивается и толщина пленки остается в пределах 1 - г - З мк. Цвет пленки зависит, главным образом, от состава обрабатываемого металла и состояния его поверхности. На полированной поверхности деталей из углеродистой стали покрытие имеет черный цвет, а на изделиях из легированной стали оно приобретает серый цвет. На опескоструенной поверхности цвет пленки изменяется от черного до темно-серого. [6]
Ввод Fe3 сдвигает потенциал стали в область пассивного состояния. Сдвиг потенциала в более положительную область за счет высокой концентрации окислителя может привести к активации стали и, следовательно, к увеличению скорости коррозии. [7]
Однако добавление этого количества озона к атмосферному воздуху с высокой концентрацией окислителей усиливает поражение, характерное для смога, а не для озона. Вероятно, содержание озона в воздухе, в дни, когда уровень окислителей к ним низок, не совсем достаточно для проявления его токсического действия, тогда как при высоких концентрациях окислителей озон реагирует преимущественно с другими компонентами атмосферы, образуя избыток токсических веществ смога. [8]
Это объясняется тем, что в кинетическом уравнении для V имеется по крайней мере один член более высокого порядка по окисляющему агенту, чем в соответствующем уравнении для соединения III. При высокой концентрации окислителя наблюдается преимущественное образование V, однако при низкой концентрации окислителя, добавляемого за 20 час, скорость образования V уменьшается и главным продуктом реакции становится соединение III. [9]
Концентрированная перекись водорода обладает тем же общим окислительным действием, которое было отмечено для более слабых ее растворов. Однако переход от свойств водных растворов перекиси водорода к свойствам чистой перекиси водорода, содержащей относительно небольшое количество воды, связан с проявлением специфических свойств мощного окислительного агента. Такие свойства ее, как большая растворимость в органических жидкостях, высокая концентрация окислителя и относительно небольшое содержание воды, приводят к тому, что в уже известных процессах, проводимых с перекисью водорода, применение концентрированной перекиси ведет к увеличению эффективности и открывает, кроме того, новые возможности ее применения. Важными факторами, регулирующими реакцию перекиси водорода и дающими ей определенное направление, являются концентрация водородных ионов, наличие и природа катализатора, а также температура. Путем надлежащего выбора растворителя имеется возможность видоизменять действие концентрированной перекиси водорода. Так, применяя алифатические кислоты в качестве растворителей, можно получить характерные реакции надкислот. [10]
Найдено, что все ионы переходных металлов, которые взаимодействуют со способными енолизироваться алифатическими альдегидами, могут также быть использованы для окисления кетонов и нитропарафинов, хотя с этими веществами они реагируют медленнее. Например, для окисления альдегидов можно использовать феррицианид калия в бикарбонатном буфере, но чтобы с такой же скоростью окислить ацетон, в качестве основного катализатора необходим едкий натр. Когда было найдено, что все эти одноэлектронные процессы окисления кетонов катализируются кислотами и основаниями, то некоторое время думали, что окислению предшествует енолиза-ция, особенно потому, что конечное окисление всегда проходит по соседней с карбонильной группой С - Н - связью, наиболее склонной к енолизации. В поддержку этой теории Драммонд и Уотерс [6] нашли, что скорость окисления циклогексанона пиро-фосфатом марганца при высокой концентрации окислителя достигает предела, который равен скорости енолизации циклогексанона. Однако недавно [7] эта идея была подвергнута сомнению, поскольку оказалось, что в сильной серной кислоте ионы как марганца, так и кобальта могут окислять кетоны со скоростями большими, чем скорости енолизации. Кроме того, изучение изотопного эффекта растворителя показывает, что в случае тех одноэлектронных окислителей, которые эффективны только в присутствии минеральной кислоты, предварительная кислотнокатализируемая реакция [ уравнение ( 2), стр. Поскольку кинетические изотопные эффекты все же наблюдаются при окислении кетонов кислыми растворами таких ионов, как Мпш, Со111 и Vv, могут протекать согласованные реакции, когда окислитель сначала координируется с атомом кислорода карбонильной группы. [11]
Для того чтобы такой элемент мог эффективно работать, следует соблюдать ряд условий. Во-первых, необходимо, чтобы в системе был деполяризатор, который восстанавливался бы с большой скоростью и мог поддерживать течение анодной реакции в питтинге. Обычно таким деполяризатором является кислород или другой окислитель. Некоторые исследователи полагают, что чем больше концентрация окислителя, тем выше будет интенсивность точечной коррозии. На самом деле, как было показано, существует какая-то оптимальная концентрация окислителя, зависящая от концентрации активатора, при которой наблюдается максимальная питтинговая коррозия. Это объясняется тем, что увеличение концентрации окислителя не только усиливает скорость катодного процесса, но одновременно уменьшает вероятность нарушения пассивного состояния в слабых местах. Кроме того, даже в большинстве точек, где началась питтинговая коррозия, при наличии высокой концентрации окислителя процесс со временем приостанавливается, очевидно, в результате частичной анодной пассивации. Лишь в тех точках, где возникающая анодная плотность тока недостаточна для того, чтобы сильно замедлить анодный процесс, коррозия с увеличением концентрации окислителя продолжает непрерывно расти вследствие большой скорости катодного процесса. [12]
Страницы: 1