Высокая концентрация - электролит
Cтраница 2
Второй член в правой части для многовалентных ионов даже для умеренно высоких концентраций электролита составляет существенную часть первого члена. В отличие от формулы ( VII.60) формула ( VII.60) никаким другим методом не выводится. [16]
Основными условиями нормального ведения процесса являются перемешивание электролита сжатым воздухом, высокая концентрация электролита и повышенная температура. [17]
Для оценки влияния активной проводимости пробы вещества использован строительный песок с высокой концентрацией электролита. [18]
Второе условие обычно хорошо выполняется во многих случаях электролиза растворов с высокой концентрацией электролита при умеренных плотностях тока с использованием растворимых анодов. [19]
Чем выше концентрация ионов, тем сильнее нарушается структура воды; при высокой концентрации электролита ближайшее окружение молекул воды состоит в основном из ионов, а не из других молекул воды. Поэтому влияние структуры воды на селективность уменьшается. Кроме того, снижается диэлектрическая постоянная среды. [20]
Известно, что индикация конечной точки титрования с применением крахмала становится менее четкой при высоких концентрациях электролитов. [21]
Таким образом, применение теории Дебая - Хюккеля ограничено разбавленными растворами, поскольку при высоких концентрациях электролита нарушается основное положение теории о существовании ионной атмосферы вокруг центрального иона. [22]
Смысл показателя кислотности рН существенно изменяется в неводных средах и даже в водных растворах с высокой концентрацией электролита, В растворах с ионной силой выше 0 1 М использование величины рН в качестве меры кислотности уже неправомерно. Существуют и другие шкалы кислотности, например функция кислотности Гаммета, которая обсуждается ниже. [23]
Разряжение в водном растворе ионов С1 -, а не ОН - в растворах с высокой концентрацией электролита также объясняется перенапряжением кислорода. Однако этого перенапряжения оказывается недостаточно, чтобы произошло разряжение ионов F - и выделение свободного фтора. [24]
Образование осадка СаСО3 в электродиализном аппарате может быть вызвано изменением рН вследствие поляризации, или существованием высокой концентрации электролита на поверхности мембран, или тем и другим вместе. Осадки такого типа обычно получаются при деминерализации воды; НСО - превращается в СО2 под действием щелочной среды в поляризационном слое и оса ждается, эффект деминерализации ухудшается проходящей одновременно концентрационной поляризацией. [25]
Покрытия па деталях, полученные в процессе осаждения Fe при пысокнх температурах, малых плотностях тока и высокой концентрации электролита, имеют гладкую бархатистую поверхность красивого серебристо-белого цвета, темнеющую после непродолжительного пребывания на воздухе. С повышением плотности тока бархатистость осадка уменьшается, сменяется слабым блеском, и при достаточно большой плотности тока покрытие становится блестящим. [26]
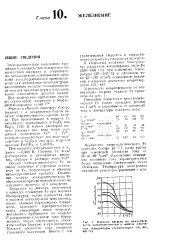 |
Влияние нагрева на мнкротвер-дость электролитического железа ( Значения температуры соответствуют 200, 400, 600 С. [27] |
Покрытия па деталях, полученные в процессе осаждения Fe при высоких температурах, малых плотностях тока и высокой концентрации электролита, имеют гладкую бархатистую поверхность красивого серебристо - Гелого цвета, темнеющую после непродолжительного пребывания на воздухе. С повышением плотности тока бархатистость осадка уменьшается, сменяется слабым блеском, и при достаточно большой плотности тока покрытие становится блестящим. [28]
 |
Влияние нагрева на микротвердость электролитического. железа ( Значения температуры соответствуют 200, 400, 600 С. [29] |
Покрытия на деталях, полученные в процессе осаждения Fe при высоких температурах, малых плотностях тока и высокой концентрации электролита, имеют гладкую бархатистую поверхность красивого серебристо-белого цвета, темнеющую после непродолжительного пребывания на воздухе. С повышением плотности тока бархатистость осадка уменьшается, сменяется слабым блеском, и при достаточно большой плотности тока покрытие становится блестящим. [30]
Страницы: 1 2 3 4