Нормальная концентрация
Cтраница 3
Нормальная концентрация раствора показывает количество грамм-эквивалентов растворенного вещества в 1 л раствора. [31]
Нормальная концентрация раствора показывает количество грамм-эквивалентов растворенного вещества в одном литре раствора. [32]
 |
Бромистое серебро с примесью бромистого кадмия в твердо-м растворе. [33] |
Нормальная концентрация дефектов CHAg IB решетке бромистого серебра относительно велика, так что всяким дополнительным разупорядочением, вызываемым давлением брома, можно пренебречь. [34]
Нормальную концентрацию выражают числом грамм-эквивалентов вещества в 1 л раствора. Чтобы вычислить грамм-эквивалент, нужно разделить грамм-молекулярную массу: 1) в случае кислоты - на проявленную ею основность в данной реакции, 2) в случае основания - на число групп ОН, принимающих участие в реакции, 3) в случае соли - на произведение числа ионов металла и его валентности. [35]
Нормальной концентрацией пользуются очень широко, так как вещества, согласно закону эквивалентов, взаимодействуют между собой в эквивалентных количествах. Эквивалентом вещества ( Э) называется такое его массовое количество, которое в данной реакции взаимодействует без остатка с одним эквивалентом любого другого вещества. [36]
Нормальной концентрацией ( или нормальностью) раствора называют число грамм-эквивалентов растворенного вещества в 1 л раствора. [37]
Понятие нормальная концентрация раствора находится в непосредственной зависимости от понятия грамм-эквивалент и является одной из основ титриметрического анализа. [38]
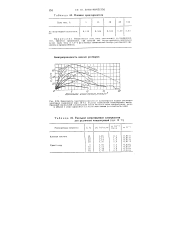 |
Плавкие предохранители.| Зависимость электропроводности от концентрации водных растворов.| Удельное сопротивление электролитов. [39] |
Указана нормальная концентрация ионов. [40]
Какова нормальная концентрация раствора H2SO4, если на титрование 0 2156 г химически чистой Na2CO3 идет 22 35 мл этого раствора. [41]
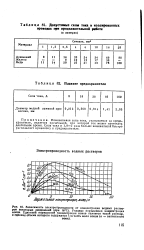 |
Допустимые силы тока в изолированных проводах при продолжительной работе.| Плавкие предохранители. [42] |
Указана нормальная концентрация ионов. [43]
 |
Формулы для взаимного пересчета концентраций раствора. [44] |
Использование нормальных концентраций позволяет рассчитать, в каких массовых отношениях растворы должны быть смешаны, чтобы растворенные вещества прореагировали без остатка, или по объемам затраченных на реакцию растворов найти их концентрации и количества прореагировавших веществ. [45]
Страницы: 1 2 3 4