Молярная концентрация - вещество
Cтраница 1
Молярная концентрация вещества с ( Х) выражается в моль / л, моль / дм, моль / см, моль / мл. [1]
Молярная концентрация вещества выражается числом молей ства в 1 дм3 ( 1 л) его. [2]
Молярные концентрации веществ принято обозначать, заключая формулы их в квадратные скобки. Например, выражения [ А ] и [ В1 означают концентрации веществ А и В, выраженные в молях на литр. [3]
Под молярной концентрацией вещества подразумевается число его грамм-молекул в 1 л раствора. [4]
Здесь и ниже абсолютные молярные концентрации вещества обозначаются их символами. [5]
Здесь квадратные скобки означают молярные концентрации веществ А и В; / г - величина, называемая константой скорости реакции, зависящая от природы реагирующих веществ и от температуры, но независящая от концентрации. Смысл кинетического уравнения состоит в том, что вероятность столкновения реагирующих молекул тем выше, чем больше их концентрации. [6]
Может случиться, что истинная молярная концентрация вещества неизвестна, например, в случае многокомпонентных растворов или растворов веществ неизвестного строения. В таких случаях величину п следует считать пропорциональной произведению толщины слоя раствора на вес растворенного вещества в данном объеме раствора. [7]
Моль на кубический метр равен молярной концентрации вещества в растворе, при которой в объеме раствора 1 м3 содержится количество растворенного вещества 1 моль. [8]
Моль на кубический сантиметр равен молярной концентрации вещества в растворе, при которой в объеме раствора 1 см3 содержится количество растворенного вещества 1 моль. [9]
При химическом равновесии отношение произведения молярных концентраций веществ, получающихся при реакции [ C ] c [ D ] d к произведению молярных концентраций исходных веществ [ А ] а [ В ] ь есть постоянная величина для данного химического процесса при заданных условиях протекания реакции. [10]
Моль на кубический метр равен молярной концентрации вещества в растворе, при которой в объеме раствора 1 м3 содержится количество растворенного вещества, равное 1 моль. [11]
Константа равновесия может быть выражена через молярные концентрации веществ, участвующих в реакции. [12]
С помощью констант скорости kt, молярных концентраций веществ Ci, а также концентрации хлора можно описать скорости образования возникающих веществ, если предположить, что в каждый момент времени реакция имеет первый порядок по каждому из реагентов. [13]
А ] и [ В ] - молярные концентрации веществ А и В и k - коэффициент пропорциональности ( константа скорости), который выражает зависимость скорости реакции от природы реагирующих веществ. [14]
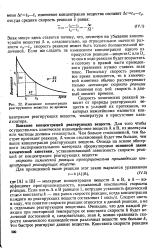 |
Изменение концентрации реагирующего вещества во времени. [15] |
Страницы: 1 2 3