Равновесная концентрация - метан
Cтраница 1
 |
Равновесная концентрация окиси углерода как функция температуры, давления и отношения пар. метан. [1] |
Равновесная концентрация метана как функция температуры, давления и отношения пар: метан. [2]
С ростом равновесной концентрации метана повышается его абсолютная концентрация при прочих одинаковых условиях. [3]
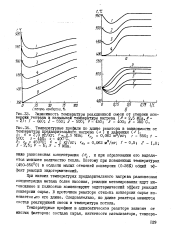 |
Зависимость температуры реакционной смеси от степени конверсии гептана и начальной температуры нагрева ( Р 2 5 МПа, / Г 2. / - 600. 2 - 550. 3 - 500. 9 - 450. S - 400. 6 - 350 С. [4] |
При низких температурах предварительного нагрева равновесная концентрация метана более высокая, реакции метанирования идут интенсивнее и полностью компенсируют эндотермический эффект реакций конверсии сырья. В проточном реакторе - степень конверсии сырья изменяется по его длине. Следовательно, по длине реактора меняются состав реагирующей смеси и температура потока. [5]
Показателем работы шахтного реактора является степень достижения равновесной концентрации метана в конвертированном газе. [6]
В случае газификации при 1400 С и 30 am равновесная концентрация метана в продуктовом газе не превышает примерно 0 02 мол. Однако равновесная концентрация метана сильно зависит от температуры: при указанных условиях она достигает 0 2 - 0 3 мол. [7]
В табл. 27 приведены результаты расчета по этому уравнению равновесной концентрации метана над углеродом для температур 327 - 1727 С. [8]
Некаталитическая автотермическая конверсия осуществляется при таких температурах, которым соответствует исче-зающе малая равновесная концентрация метана. [9]
Принт [22] накалива /: током различные образцы угля и определял равновесную концентрацию метана в смеси с водородом, устанавливающуюся над ними. В опытах с платинированным углем при атмосферном давлении были получены следующие результаты. [10]
Для аморфного углерода, таким образом, получается более высокая по сравнению с графитом, равновесная концентрация метана. [11]
Этот процесс формально можно рассматривать как паровую конверсию углеводородов, проводимую при параметрах, которые определяют высокую равновесную концентрацию метана. Аналогично расчету паровой конверсии углеводородов расчет химического равновесия их метанирования можно свести простым и немногочисленным операциям. [12]
 |
Зависимость содержания.| Зависимость содержания окиси углерода в газе от давления и температуры при реакции С СО2 2СО - Q. [13] |
Кривые I и II показывают изменение равновесной концентрации окиси углерода, кривые III и IV - изменение равновесной концентрации метана. Кривые ( рис. 137) свидетельствуют о значительном влиянии температуры на сдвиг равновесия реакций газификации твердого топлива и подтверждают, что для увеличения выхода продуктов газификации при эндотермических реакциях необходимы высокие температуры, при экзотермических - низкие. [14]
Высокотемпературную некаталитическую конверсию метана под давлением ведут при той же температуре, что и под атмосферным давлением, так как при столь высоких температурах равновесные концентрации метана ничтожно малы. [15]
Страницы: 1 2