Равновесная концентрация - вещество
Cтраница 3
Полученные нами зависимости между равновесной концентрацией вещества в твердой и жидкой фазах в первом приближении выражаются уравнением типа уравнения Лэнгмюра. [31]
Если легко и точно находятся равновесные концентрации веществ и, следовательно, константа равновесия, то уравнение ( IX. [32]
 |
Диаграмма зависимости коэффициентов активности ионов от ионной силы раствора 22. [33] |
Концентрационная константа К выражается через равновесные концентрации веществ ( ионов), участвующих в равновесии. [34]
 |
Изотермы абсорбции. [35] |
Кривая, выражающая зависимость между равновесной концентрацией вещества в объеме и количеством его на поверхности адсорбента при постоянной температуре, называется изотермой адсорбции. Уравнение ( 290) является уравнением изотермы адсорбции. [36]
Формулировка его такова: отношение произведений равновесных концентраций веществ правой и левой частей уравнения обратимого химического процесса представляет постоянную величину, независимую от тех условий, при которых осуществляется равновесие, если только температура остается постоянной, а концентрации возведены в степень их стехиометрических коэффициентов. [37]
Обычно определяемой величиной является не активность, а равновесная концентрация вещества. Поэтому при выполнении расчетов удобно использовать концентрационные константы равновесия. [38]
 |
Распределение вещества между двумя несмешивающимися растворителями ( концентрация в молях на литр. [39] |
Следовательно, при Р, Т const отношение равновесных концентраций вещества, распределенного между двумя фазами, не зависит от общего количества его. [40]
Экспериментальное изучение химического равновесия в конечном счете сводится к определению равновесных концентраций веществ в реакционной смеси и определению константы равновесия. [41]
Введение порции чистого газа в сосуд приводит к уменьшению достигнутого значения равновесной концентрации вещества в газовой фазе, поэтому отбор следует производить многократной прокачкой шприца в течение времени, достаточного для восстановления рав новесия в системе. [42]
Величина К представляет константу равновесия данной реакции и равняется отношению произведения равновесных концентраций веществ, получившихся в результате реакции, к произведению равновесных концентраций веществ, вступающих в реакцию. [43]
Эти простые правила облегчают составление и преобразование системы уравнений для расчета равновесных концентраций веществ - в газовой фазе. [44]
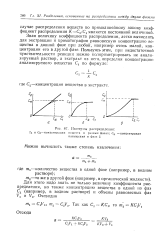 |
Изотермы распределения. [45] |
Страницы: 1 2 3 4