Равновесная концентрация - водород
Cтраница 1
Незначительная равновесная концентрация водорода при восстановлении РегОз до Fe3O4 не позволяет экспериментально уловить влияния их взаимной растворимости. [1]
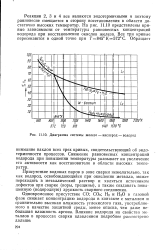 |
Диаграмма системы железо - кислород - водород. [2] |
Снижение равновесных концентраций водорода при повышении температуры указывает на увеличение его активности как восстановителя в области высоких температур. [3]
 |
Влияние температуры на степень диссоциации а различных газов. [4] |
Графики равновесных концентраций водорода и азота в стали, алюминии, никеле и меди при различных температурах, приведенные на рис. 1.23, а, б, показывают, что в жидком металле равновесные концентрации отдельных газов весьма значительны, а при переходе в твердое состояние резко падают, несмотря на его высокую температуру. Это создает риск образования пор при ускоренной кристаллизации. [5]
С - равновесная концентрация водорода; 1 / - - объем жидкой фазы; Т - температура; X - концентрация катализатора. [6]
В таблице 2 приведены равновесные концентрации водорода в циркулирующем газе в зависимости от температуры и объемной скорости подачи сырья при циркуляции газа 600 нм3 / м3 сырья и общем давлении 15 эти. [7]
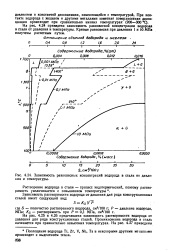 |
Зависимость равновесных концентраций водорода в стали от давления и температуры. [8] |
На рис. 4.24 приведена зависимость равновесной концентрации водорода в стали от давления и температуры. Кривые равновесия при давлении I и ГО МПа получены расчетным путем. [9]
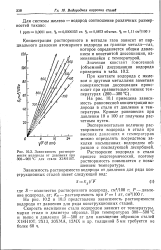 |
Зависимость растворимости водорода от давления при 300 - 900 С для стали Х18Н10Т. [10] |
На рис. 10.1 приведена зависимость равновесной концентрации водорода в стали от давления и температуры. Кривые равновесия при давлении 10 и 100 ат получены расчетным путем. [11]
Авторы указывают, что увеличение равновесной концентрации водорода ( третья колонка) зависит не только от снижения количества водорода на связывание серы, но и от некоторого форсирования процессов дегидрогенизации нафтенов с температурой. [12]
В результате уменьшится равновесная концентрация водяного пара и увеличатся равновесные концентрации водорода и кислорода. [13]
 |
Зависимость равновесного парциального давления водорода от температуры для титана с различным содержанием водорода, %. [14] |
Изменение температуры или давления водорода смещает равновесие в ту или другую сторону до тех пор, пока не установится равновесная концентрация водорода, соответствующая новым условиям. Повышение температуры или уменьшение давления в системе приводит к понижению концентрации водорода в металле. На этом основано удаление водорода из титана и его сплавов с помощью вакуумного отжига. [15]
Страницы: 1 2 3