Текущая концентрация - реагирующее вещество
Cтраница 1
Текущие концентрации реагирующих веществ невозможно применять в расчетах, поэтому движущую силу выражают через начальные концентрации реагирующих веществ и степень превращения их. [1]
С - текущая концентрация реагирующего вещества, зависящая от расстояния х от поверхности куска катализатора; S - внутренняя поверхность. [2]
Бели известны скорость диффузии шдиф, исходная и текущая концентрация реагирующих веществ С0 и С, толщина диафрагмы р ( в см) и ее сечение b ( в см2), концентрацию С можно определить, разделив скорость диффузии на скорость потока и газа, поступающего за диафрагму. [3]
 |
График для определения времени контактирования ( к примеру 1. [ IMAGE ] График для определения времени контактирования ( к примеру 2. [4] |
Скорость реакции и & СыоСо2 - Выразим текущие концентрации реагирующих веществ через число прореагировавших молей и начальные концентрации. [5]
В ряде случаев кинетические константы определяются по текущим концентрациям реагирующих веществ, однако это не должно отразиться на общности описываемого метода. [6]
CtK - конечные концентрации реагирующих веществ; Сь Ci, С3 - - текущие концентрации реагирующих веществ. [7]
С ( - - конечные концентрации реагирующих веществ; С, С /, С; - текущие концентрации реагирующих веществ. [8]
Здесь w - скорость протекания реакции; & - константа скорости реакции, зависящая от температуры и химической природы реагирующих веществ; С А, Св - соответствующие текущие концентрации реагирующих веществ Л и В в смеси; ш, п - числа молей реагирующих веществ. [9]
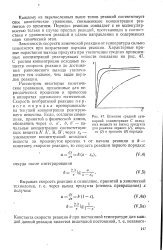 |
Влияние средней суммарной концентрации С исходных веществ на выход продукта для реакции первого ( /, второго ( 2 и третьего ( 3 порядка. [10] |
Рассмотрим некоторые кинетические уравнения, применимые для периодических процессов и процессов в аппаратах идеального вытеснения. Скорость необратимой реакции первого порядка пропорциональна текущей концентрации реагирующего вещества. [11]
В главе II изложены основы математического описания и моделирования применительно к задачам масштабирования и автоматизации химических процессов и обосновывается возможность получения кинетических данных в ограниченной ( локальной) области изменения параметров. В общем случае в качестве уравнений локальной кинетики рекомендуется использовать известные уравнения химической кинетики, введя в них зависимость от факторов, функционально связанных с текущей концентрацией реагирующих веществ. [12]
В главе II изложены основы математического описания и моделирования применительно к задачам масштабирования и автоматизации химических процессов и обосновывается возможность получения кинетических данных в ограниченной ( локальной) области изменения параметров. В общем случае в качестве уравнений локальной кинетики рекомендуется использовать известные уравнения химической, кинетики, введя в них зависимость от факторов, функционально связанных с текущей концентрацией реагирующих веществ. [13]
С ростом концентрации исходных веществ скорость реакции до достижения равновесного выхода увеличивается тем сильнее, чем выше порядок реакции. Рассмотрим некоторые кинетические уравнения для периодических процессов и процессов в аппаратах идеального вытеснения. Скорость необратимой реакции первого порядка пропорциональна текущей концентрации реагирующего вещества. [14]
Страницы: 1