Концентрирование - катион
Cтраница 1
Концентрирование катионов и анионов может проводиться как из водных растворов смеси электролитов, так и из водных растворов смеси электролитов и неэлектролитов. [1]
Для концентрирования катионов применяют катио-ниты КУ-2 или СБС, измельченные до размера зерен около 0 05 - 0 2 мм. Катионит заливают водой и оставляют до следующего дня для набухания. [2]
Метод основан на концентрировании катионов в процессе электролиза на стационарном ртутном электроде в виде висящей капли ртути с последующей регистрацией катионов, выделившихся из амальгамы при ее окислении. [3]
Ионный обмен широко используют для концентрирования катионов и анионов из разбавленных растворов. Для этого сначала большой объем очень разбавленного раствора ( несколько литров) пропускают через слой катионита, сорбирующего все катионы. Затем вытесняют их из катионита возможно меньшим объемом хлороводородной кислоты, т.е. получают фильтрат объемом в несколько миллилитров. Таким образом удается повысить концентрацию определяемых ионов в десятки и сотни раз. [4]
Ионный обмен широко используют для концентрирования катионов и анионов из разбавленных растворов. Принцип этого приема состоит в следующем. Сначала большой объем очень разбавленного раствора ( несколько литров) пропускают через слой катионита, сорбирующего все катионы. Таким образом удается повысить концентрацию определяемых ионов в десятки и сотни раз. [5]
Ионный обмен широко используют для концентрирования катионов и анионов из разбавленных растворов. Для этого сначала большой объем очень разбавленного раствора ( несколько литров) пропускают через слой катионита, сорбирующего все катионы. Таким образом удается повысить концентрацию определяемых ионов в десятки и сотни раз. [6]
Сулъфокислотный катионит в КН4 - форме использовали для концентрирования катионов морской воды. Смейлс и Сэлмон [54] разработали метод определения рубидия и цезия, основанный на нейтронном активировании получающихся при этом концентратов. [7]
Из приведенных в таблице данных видно, что, применяя концентрирование катионов при помощи ионитов в динамических условиях, можно увеличить чувствительность реакций с органическими реагентами в 5 - 25 раз. Существенное повышение чувствительности реакций обычно достигается и при извлечении ионов из раствора в статических условиях. [8]
Грабб и Земан [ G51 ] использовали маленькие кусочки катио-нитовой мембраны для концентрирования катионов для спектрографических определений. Они нашли, что этим методом может быть определен 1 мкг кабальта с точностью 0 1 мкг. [9]
Исследование ионообменных свойств серпентинита открывает новые возможности использования этого природного сорбента для разделения и концентрирования катионов. Представляет интерес изучение анионооб-менных свойств серпентинита. [10]
Больше всего внимания было уделено обработке сбросов водородными или натриевыми катионообменными смолами в целях концентрирования катионов меди и цинка. Одной из причин того, почему до сих пор не имеется соответствующих промышленных установок, является высокая стоимость регенерирующего раствора и быстрая амортизация оборудования в связи с высоким содержанием в этих сбросах натрия, кальция, магния и сульфатов. [11]
В настоящее время в химкон-троле на паросиловых установках единственным надежным методом определения малых солесодержа-ний станционных вод является концентрирование катионов на ионообменной смоле. Полученный кислый регенерат обычно содержит катионы натрия, кальция, магния, железа, алюминия, цинка, меди, аммиака и ряд других катионов. Так как число катионов, сконцентрированных в кислом регенерате, велико, а общая их концентрация ничтожно мала, более или менее полный анализ полученного концентрата представляет определенную трудность. [12]
Не следует применять резиновые трубки для подачи и отвода кислоты при регенерации лабораторных Н - катионитных фильтров для анализа вод типа конденсата методом концентрирования катионов, так как при этом получаются завышенные результаты, в особенности по кальцию. [13]
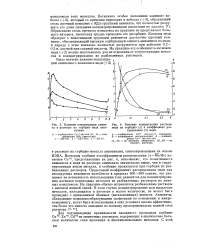 |
Влияние концентрации аммиака в растворе на сорбцию меди анио-нитами.| Влияние концентрации раствора меди на сорбцию ( 1 и коэффициент распределения ( 2 меди. [14] |
Изотермы сорбции и коэффициенты распределения ( аМе / Ме) катионов Си4 2, представленные на рис. 4, показывают, что селективность анионитов к меди из раствора аммиаката значительно выше, чем к гидра-тированным ионам металла, и особенно проявляется при сорбции из разбавленных растворов. Предельный коэффициент распределения меди для исследуемых анионитов колеблется в пределах 400 - 500 единиц, что указывает на возможность использования этих анионитов для концентрирования катионов переходных металлов из разбавленных растворов их амин-ных комплексов. На практике обычно встречаются разбавленные растворы с высокой ионной силой. В этом случае концентрирование или выделение металлов, находящихся в растворе в малом количестве, не может быть проведено с применением обычных ( неселективных) ионитов. [15]
Страницы: 1